��Ŀ����
5����ҵ�ϽӴ�������������У��ڷ���¯������������ ����Ҫ�ɷ�ΪFeS2���Ļ�ѧ����ʽΪ��4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$2Fe2O3 +8SO2����ش��������⣺��1����֪SΪ-1�ۣ���������Ԫ������Ԫ�غ���Ԫ�أ�
��2��������1.0t�����������ʺ���Ϊ30%�������в�����Ԫ�أ�����FeS2��ת����Ϊ90%�����״���£����ɵ�SO2���Ϊ321m3��
��3�������������ղ���֣���¯���л���+2�۵���Ԫ�أ������һ����ʵ��֤��֮������ʵ��������йص�ʵ������ ����ѡ����Լ���ϡ���ᡢKMnO4��Һ��Ʒ����Һ��NaOH��Һ�ȣ�
��4��¯�����ᴿ���Ƶ�FeCl3�����ӹ�ҵ��Ҫ��30%��FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ����ӡˢ��壮
����д��FeCl3��Һ��ͭ��Ӧ�Ļ�ѧ����ʽ��2FeCl3+Cu�T2FeCl2+CuCl2��
�ڼ��鷴Ӧ�����Һ�д���Fe3+���Լ�����KSCN��Һ��
�����Ӹ�ʴ��ķ�Һ�л���ͭ�����»��FeCl3��Һ�������Լ��У���Ҫ�õ���һ���ǣ�����ĸ��A��
������ˮ ������ ��Ũ���� ��ϡ ���� ��Ũ��ˮ ����ˮ
A���٢ڢܢ�B���٢ۢܢ�C���ڢܢ�D���٢ܢ�
���� ��1��SΪ-1�ۣ�����Ϊ+2�ۣ��÷�Ӧ����Ԫ�غ���Ԫ�صĻ��ϼ۶����ߣ��ڷ�Ӧ�б�������
��2�����ݷ�Ӧ����ʽ����������ݼ�������ɵĶ�������������
��3�������������ӣ�ͨ��ʹ�����Ը��������Һ����Ҫ��ϡ�����ܽ���Ʒ���ݴ����ʵ�鷽����
��4����ͭ���Ȼ�����Ӧ�����Ȼ������Ȼ�������
�ڼ�����Һ��Fe3+����ͨ����KSCN��Һ����Һ���˵��Fe3+���ڣ�
�۸������ù������۽�������ת����ͭ���ʣ�Ȼ������������ĵ����������ۣ��ټ�����ˮ���������ӻ�ԭ�������ӣ��ݴ�ѡ��ʹ�õ��Լ���
��� �⣺��1����Ӧ4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$2Fe2O3 +8SO2�У�FeS2��SԪ��Ϊ-1�ۣ�����Ԫ��Ϊ+2�ۣ���Ӧ������+3�۵���������+4�۵�S������Ԫ�غ���Ԫ���ڷ�Ӧ�ж���������
�ʴ�Ϊ����Ԫ�غ���Ԫ�أ�
��2��������1.0t�����������ʺ���Ϊ30%�������в�����Ԫ�أ�����FeS2��ת����Ϊ90%����
4FeS2+11O2 $\frac{\underline{\;����\;}}{\;}$2Fe2O3 +8SO2��
352g 8��22.4L
1��106g����1-30%����90% V��SO2��
��V��SO2��=$\frac{22.4L��8��1��1{0}^{6}g����1-30%����90%}{352g}$=3.21��105L=321m3��
�ʴ�Ϊ��321��
��3�������������ղ���֣���¯���л���+2�۵���Ԫ�أ�����ϡ���ܽ�����ɵ��������Ӿ��л�ԭ�ԣ���KMnO4��Һ����ǿ�����ԣ���ʹKMnO4��Һ��ɫ����ѡ���Լ�Ϊϡ���ᡢKMnO4��Һ��
��������������Ϊ��ȡ������������ϡ���ᣬȻ��μ�KMnO4��Һ���۲쵽��ҺʹKMnO4��Һ��ɫ����֤��¯���л���+2�۵���Ԫ�أ�
��ȡ������������ϡ���ᣬȻ��μ�KMnO4��Һ���۲쵽��ҺʹKMnO4��Һ��ɫ����֤��¯���л���+2�۵���Ԫ�أ�
��4����ͭ���Ȼ�����Ӧ�����Ȼ������Ȼ���������Ӧ����ʽΪ��2FeCl3+Cu�T2FeCl2+CuCl2��
�ʴ�Ϊ��2FeCl3+Cu�T2FeCl2+CuCl2��
�ڼ�����Һ��Fe3+����ͨ����KSCN��Һ��ȡ������Һ���Թ��У��μ�KSCN��Һ����Һ���˵��Fe3+���ڣ�
�ʴ�Ϊ��KSCN��Һ��
�۸�ʴ��Һ�к����Ȼ�ͭ���Ȼ������Լ��Ȼ�������������������Ժ��Ȼ�����Ӧ�����Ȼ����������Ȼ�ͭ��Ӧ���ɽ���ͭ���Ȼ���������Fe+Cu2+=Fe2++Cu��Fe+2Fe3+=3Fe2+�����ˣ����õ���Һ���Ȼ������������ǽ���ͭ����������ͭ�������ᷴӦ�������������ԣ�Fe+2H+=Fe2++H2�����������м���������������Խ�ͭ���룬�ٹ��ˣ��õ�����Һ���Ȼ��������������������ԣ��ܽ�������������Ϊ��������2Fe2++Cl2=2Fe3++2Cl-���������Һ��ͨ���������ɣ���ѡ�õ��Լ��У�������ˮ�������ۡ���ϡ���ᡢ����ˮ��
�ʴ�Ϊ��A��
���� ���⿼������ʵ�鷽������ƣ���Ŀ�Ѷ��еȣ��漰��ѧ����ʽ��д����ѧ����ʽ���㡢���ʷ�����ơ�������ԭ��Ӧ�жϡ��������Ӽ��鷽��֪ʶ����ȷ������������Ϊ���ؼ�������������ѧ���ķ�����������ѧ���㡢��ѧʵ��������

 �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д�| A�� | �ӻ�������Բ���м����γ� | |
| B�� | �ӻ�ǰ��Ĺ�������䣬���������״�����˸ı� | |
| C�� | ���ۼ����з����� | |
| D�� | ��̬Naԭ�Ӻ������ռ��3���ܲ㡢4���ܼ���6��ԭ�ӹ����6�ֵ����˶�״̬ |
| A�� |  ʯ�͵ķ��� | B�� |  �γ�ԭ��� | C�� |  ���Ƶý����� | D�� |  ��ȡ�������� |
| A�� | ����NaOH��Һ��Ӧ��1mol�����ʿ���4mol NaOH��Ӧ | |
| B�� | ������ˮ��Ӧ����1mol��������������ˮ��Ӧ����6mol Br2 | |
| C�� | һ��������1mol�����ʿ���H2�ӳɣ���H2�����Ϊ7mol | |
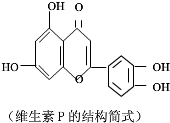
| D�� | ά����P��FeCl3��Һ������ɫ��Ӧ |
| A�� | �þ�����۷е�͡�Ӳ��С | |
| B�� | ������̼ԭ������C-O��ѧ����֮��Ϊ1��2 | |
| C�� | ����Ŀռ���С������6��ԭ�ӹ��� | |
| D�� | �þ�����̼ԭ�Ӻ���ԭ�ӵĸ�����Ϊ1��2 |
| A�� | ������C��H��O����֮��Ϊ1��2��3 | B�� | ������C��H����֮��Ϊ1��2 | ||
| C�� | �����к�����ԭ�� | D�� | ���л�������ʽΪΪCH4 |
| A�� | ���ۺ���ά�ػ�Ϊͬ���칹�壬����ˮ��Ϊ��ԭ�Ե��� | |
| B�� | �����յķ����ɼ���ë֯�����֯�� | |
| C�� | ��������Һ�м���Ũ���������Һ�г�����������ˮ��������ܽ� | |
| D�� | ��Ȼ��֬�еľ��й̶����۷е㣬ֲ���Ͳ���ʹ������Ȼ�̼��Һ��ɫ |
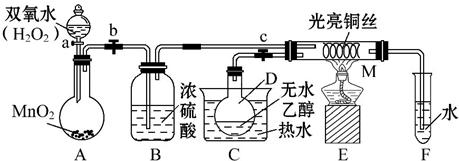
 ��ͼ��ʾ��AΪֱ����Դ��BΪ�������Ȼ�����Һ�ͷ�̪��Һ����ֽ��CΪ��Ʋۣ���ͨ��·����B�ϵ�c���Ժ�ɫ������գ�
��ͼ��ʾ��AΪֱ����Դ��BΪ�������Ȼ�����Һ�ͷ�̪��Һ����ֽ��CΪ��Ʋۣ���ͨ��·����B�ϵ�c���Ժ�ɫ������գ�