题目内容
12.下列常温下的下列物质属于所气态有机物的是 ( )| A. | CH3Cl | B. | CH2Cl2 | C. | CCl4 | D. | 苯 |
分析 常见有机物中常温下为气态有:C原子数≤4烃、新戊烷、一氯甲烷、甲醛等,据此判断.由5到16个碳组成的烷烃常温下为液态,由17个碳以上组成的烷烃常温下为固态.
解答 解:A.CH3Cl常温下是气体,故A正确;
B.CH2Cl2常温下是液体,故B错误;
C.CCl4常温下是液体,故C错误;
D.苯常温下为液态,故D错误.
故选A.
点评 本题考查了有机物的物理性质,注重了基础知识考查,注意掌握常温下为气态常见有机物,本题难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
2.下列有关元素周期表的说法正确的是( )
| A. | 第I A族元素都是碱金属元素 | |
| B. | 元素周期表中有18个纵行,所以有18个族 | |
| C. | 可以从过渡金属中寻找新型催化剂 | |
| D. | 主族元素的金属元素原子最外层电子数一定小于或等于4 |
3.下列哪位科学家最先发现了电子( )
| A. | Joseph John Thomson | B. | Ernest Rutherford | ||
| C. | Justus von Liebig | D. | Jons Jakob Berzelius |
20.下列反应属于吸热反应的是( )
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | C. | 炸药爆炸 | D. | 氧化钙溶于水 |
17.已知同温同浓度时,①H2CO3比H2S的电离(一级电离)常数大,②H2S比HCO3-的电离常数大(即H2S的K1比H2CO3的K2大),根据酸与盐的反应规律,下列反应中不正确的是( )
| A. | Na2CO3+H2S=NaHCO3+NaHS | B. | Na2S+H2O+CO2=NaHS+NaHCO3 | ||
| C. | 2NaHCO3+H2S=Na2S+2H2O+2CO2 | D. | NaHS+H20+CO2=NaHCO3+H2S |
4.下列溶液中,酸性最强的是( )
| A. | 0.01mol/L的盐酸 | B. | 0.01mol/L的醋酸溶液 | ||
| C. | c(H+)=10-3mol/L的溶液 | D. | c(OH-)=10-1mol/L溶液 |
5. 某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭 真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)?2NH3(g)+CO2(g)
实验测得的不同温度下的平衡数据列于下表:
①可以判断该分解反应已经达到平衡的是BC.
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算 25.0℃时氨基甲酸铵的分解平衡常数:K=c2(NH3)•c(CO2)=($\frac{2}{3}$c总)2($\frac{1}{3}$c总)=$\frac{4}{27}$×(4.8×10-3)3=1.6×10-8.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在 25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量增加(填“增加”、“减少”或“不变”).
④氨基甲酸铵分解反应的焓变△H>0(填“>”、“=”或“<”),熵变△S>0(填“>”、“=”或“<”).
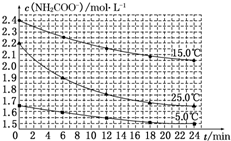
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定其水解反应速率,得到c(NH2COO-)随时间的变化趋势如图所示.
⑤计算 25.0℃时,0~6min 氨基甲酸铵水解反应的平均速率:0.05mol•L-1•min-1.
⑥根据图中信息,如何说明该水解反应速率随温度升高而增大:25.0℃时反应物的起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15.0℃时的大.
 某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭 真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s)?2NH3(g)+CO2(g)
实验测得的不同温度下的平衡数据列于下表:
| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/mol•L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算 25.0℃时氨基甲酸铵的分解平衡常数:K=c2(NH3)•c(CO2)=($\frac{2}{3}$c总)2($\frac{1}{3}$c总)=$\frac{4}{27}$×(4.8×10-3)3=1.6×10-8.
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在 25.0℃下达到分解平衡.若在恒温下压缩容器体积,氨基甲酸铵固体的质量增加(填“增加”、“减少”或“不变”).
④氨基甲酸铵分解反应的焓变△H>0(填“>”、“=”或“<”),熵变△S>0(填“>”、“=”或“<”).
(2)已知:NH2COONH4+2H2O?NH4HCO3+NH3•H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定其水解反应速率,得到c(NH2COO-)随时间的变化趋势如图所示.
⑤计算 25.0℃时,0~6min 氨基甲酸铵水解反应的平均速率:0.05mol•L-1•min-1.
⑥根据图中信息,如何说明该水解反应速率随温度升高而增大:25.0℃时反应物的起始浓度较小,但0~6min的平均反应速率(曲线的斜率)仍比15.0℃时的大.
6.检验SO2中是否有CO2,应采取的措施是( )
| A. | 通过澄清石灰水 | |
| B. | 通过Ba(OH)2溶液再通过石灰水 | |
| C. | 通过酸性高锰酸钾溶液再通过石灰水 | |
| D. | 通过小苏打悬浊液再通过石灰水 |
 .
.