题目内容
13.下列实验能获得成功的是( )| A. | 用溴水可鉴别苯、乙醇、苯乙烯 | |
| B. | 将乙烷和氯气的混合气放在光照条件下反应制备氯乙烷(C2H5Cl) | |
| C. | 苯、溴水、铁粉混合制成溴苯 | |
| D. | 检验氯代烃中含氯,加NaOH溶液加热后,用稀硫酸酸化,再检验 |
分析 A.苯与溴水发生萃取分层,乙醇与溴水互溶,苯乙烯与溴水发生加成反应使其褪色;
B.光照下取代反应为链锁反应,产物复杂;
C.苯与溴水不反应;
D.检验卤素离子,水解后加硝酸酸化.
解答 解:A.苯与溴水发生萃取分层,乙醇与溴水互溶,苯乙烯与溴水发生加成反应使其褪色,现象不同,可鉴别,故A正确;
B.光照下取代反应为链锁反应,产物复杂,则光照条件下反应制备纯净的氯乙烷(C2H5Cl),故B错误;
C.苯与溴水不反应,应选苯、液溴、铁粉混合制成溴苯,故C错误;
D.检验卤素离子,水解后加硝酸酸化,硫酸银为沉淀,则不能选硫酸酸化,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的性质、鉴别、制备实验为解答本题的关键,侧重分析与实验能力的考查,注意有机物性质的应用,题目难度不大.

练习册系列答案
相关题目
14.NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 1molCl2与足量Fe反应,转移的电子数为2NA | |
| B. | 标准状况下,22.4LSO3所含的分子数为NA个 | |
| C. | 足量铜与11.18mol/L浓硫酸反应可以得到SO2的分子数总数为9NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去电子数为2NA |
5.已知还原性:SO32->I-.向含有amolKI和amolK2SO3的混合液中通入bmolCl2充分反应(不考虑Cl2与I2之间的反应).下列说法不正确的是( )
| A. | 当a≥b时,发生的离子反应为SO32-+Cl2+H2O=SO42-+2H++2Cl- | |
| B. | 当5a=4b时,发生的离子反应为SO32-+2I-+5Cl2+4H2O=4SO42-+I2+8H++10Cl- | |
| C. | 当a≤b≤$\frac{3}{2}$a时,反应中转移电子的物质的量n(e-)为amol≤n(e-)≤3amol | |
| D. | 当a<b<$\frac{3}{2}$a时,溶液中SO42-、I-与Cl-的物质的量之比为a:(3a-2b):2b |
 向恒容密闭容器中充入2.0mol A和3.0mol B,发生反应xA(g)+2B(g)?yC(g).恒温下反应10min后突然改变某一条件,12min时达到化学平衡状态I;18min时升高温度,22min时达到化学平衡状态II.容器中A、C的物质的量浓度随时间变化的曲线如图所示,请根据题给信息回答下列问题:
向恒容密闭容器中充入2.0mol A和3.0mol B,发生反应xA(g)+2B(g)?yC(g).恒温下反应10min后突然改变某一条件,12min时达到化学平衡状态I;18min时升高温度,22min时达到化学平衡状态II.容器中A、C的物质的量浓度随时间变化的曲线如图所示,请根据题给信息回答下列问题: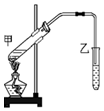 某学习小组为探究乙醇与乙酸的酯化反应,在试管甲中加入3ml乙醇,然后边振荡试管边慢慢加入2ml浓硫酸和2ml乙酸;按如图连接好装置,用酒精灯缓慢加热,将产生的蒸气经导管通到乙试管内的液面上.按要求填空:
某学习小组为探究乙醇与乙酸的酯化反应,在试管甲中加入3ml乙醇,然后边振荡试管边慢慢加入2ml浓硫酸和2ml乙酸;按如图连接好装置,用酒精灯缓慢加热,将产生的蒸气经导管通到乙试管内的液面上.按要求填空: