题目内容
下列各组中的两种物质相互作用时,改变反应条件或反应物的用量,不会影响产物组成的是( )
| A、Na与O2 |
| B、NaOH与CO2 |
| C、NaOH与AlCl3 |
| D、Na2O与CO2 |
考点:钠的化学性质,钠的重要化合物
专题:金属概论与碱元素
分析:A.钠和氧气在没有条件或燃烧条件时产物不同;
B.氢氧化钠和二氧化碳反应,二氧化碳的量不同,其产物不同;
C.氯化铝和少量氢氧化钠溶液反应生成白色沉淀,和过量氢氧化钠溶液反应时先生成沉淀后沉淀溶解;
D.过氧化钠和二氧化碳反应,无论二氧化碳是否过量,都只生成碳酸钠.
B.氢氧化钠和二氧化碳反应,二氧化碳的量不同,其产物不同;
C.氯化铝和少量氢氧化钠溶液反应生成白色沉淀,和过量氢氧化钠溶液反应时先生成沉淀后沉淀溶解;
D.过氧化钠和二氧化碳反应,无论二氧化碳是否过量,都只生成碳酸钠.
解答:
解:A.钠和氧气在没有条件的条件下反应生成氧化钠,钠在空气中燃烧生成过氧化钠,所以与反应条件有关,故A不选;
B.氢氧化钠溶液和少量二氧化碳反应生成碳酸钠,和过量二氧化碳反应生成碳酸氢钠,所以与反应物用量有关,故B不选;
C.氯化铝和少量氢氧化钠溶液反应生成氢氧化铝白色沉淀,和过量氢氧化钠溶液反应时,先生成氢氧化铝沉淀,然后氢氧化铝再和氢氧化钠反应生成可溶性的偏铝酸钠,溶液又变澄清,所以与反应物用量有关,故C不选;
D.无论二氧化碳是否过量,过氧化钠和二氧化碳反应都只生成碳酸钠,所以与温度、反应物用量无关,故D选;
故选D.
B.氢氧化钠溶液和少量二氧化碳反应生成碳酸钠,和过量二氧化碳反应生成碳酸氢钠,所以与反应物用量有关,故B不选;
C.氯化铝和少量氢氧化钠溶液反应生成氢氧化铝白色沉淀,和过量氢氧化钠溶液反应时,先生成氢氧化铝沉淀,然后氢氧化铝再和氢氧化钠反应生成可溶性的偏铝酸钠,溶液又变澄清,所以与反应物用量有关,故C不选;
D.无论二氧化碳是否过量,过氧化钠和二氧化碳反应都只生成碳酸钠,所以与温度、反应物用量无关,故D选;
故选D.
点评:本题考查了反应物间反应条件或反应物用量与反应产物的联系,题目难度不大,注意把握常见元素化合物的性质,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )
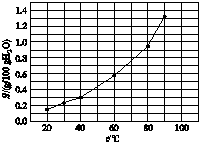

| A、60℃时溴酸银的Ksp约等于6×10-4 |
| B、温度升高时溴酸银溶解速度加快 |
| C、溴酸银的溶解时放热过程 |
| D、若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 |
下列说法正确的是( )
A、按系统命名法, 的名称为2,4,5-三甲基己烷 的名称为2,4,5-三甲基己烷 |
B、分子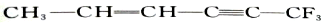 中,位于同一平面上碳原子最多有6个 中,位于同一平面上碳原子最多有6个 |
C、化合物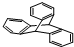 是苯的同系物 是苯的同系物 |
| D、3-甲基-3-乙基戊烷的一氯取代产物有6种 |
设NA为阿伏加德罗常数.下列说法正确的是( )
| A、1L 1mol?L-1的NaClO 溶液中含有ClO-的数目为NA |
| B、1mol Mg在空气中燃烧被完全氧化生成MgO和Mg3N2,失去2NA个电子 |
| C、标准状况下,22.4L苯含有1NA个苯分子 |
| D、1mol的羟基与1mol的氢氧根离子所含电子数均为9NA |
中和滴定是一种操作简单,准确度高的定量分析方法.实际工作中也可利用物质间的氧化还原反应、沉淀反应进行类似的滴定分析,下列有关几种具体的滴定分析(待测液置于锥形瓶内)的说法不正确的是( )
| A、用标准酸性KMnO4溶液滴定Na2SO3溶液以测量其浓度:滴定终点时,溶液由无色变为紫红色 |
| B、利用“Ag++SCN-═AgSCN↓”反应,用标准KSCN溶液测量AgNO3溶液浓度时可用Fe(NO3)3作指示剂 |
| C、利用“2Fe3++2I-═I2+2Fe2+”,用FeCl3溶液测量KI样品中KI的百分含量时可用淀粉作指示剂 |
| D、用标准NaOH溶液测量某盐酸溶液的浓度时,若用酚酞作指示剂,当观察到溶液由无色变红色,且半分钟不恢复时达到滴定终点 |