题目内容
16.下列各物质加到或通入硝酸银溶液里能使溶液变浑浊的是( )| A. | CH3CH2Cl | B. | CO2 | C. | Cl2 | D. | NaNO3 |
分析 加到或通入硝酸银溶液里能使溶液变浑浊说明能够溶于水且与硝酸银电离产生的银离子发生反应生成不溶性沉淀,据此分析解答.
解答 解:A.CH3CH2Cl为有机物,不溶于水,属于非电解水,与硝酸银不反应,溶液不会变浑浊,故A不选;
B.碳酸的酸性弱于硝酸,二氧化碳与硝酸银溶液不反应,溶液不会变浑浊,故B不选;
C.氯气通入硝酸银溶液,先与水反应生成盐酸和次氯酸,盐酸与硝酸银反应生成氯化银白色沉淀,溶液变浑浊,故C选;
D.硝酸钠与硝酸银溶液不反应,溶液不会变浑浊,故D不选;
故选:C.
点评 本题考查了元素化合物知识,明确氯气的性质及氯水的成分是解题关键,题目难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
6.HPE是合成除草剂的重要中间体,其结构简式如图所示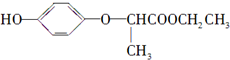 下列有关HPE的说法正确的是( )
下列有关HPE的说法正确的是( )
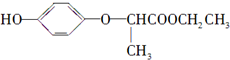 下列有关HPE的说法正确的是( )
下列有关HPE的说法正确的是( )| A. | 1 mol HPE最多可和2 mol NaOH反应 | |
| B. | HPE不能跟浓溴水反应 | |
| C. | HPE不能发生加成反应 | |
| D. | HPE在核磁共振氢谱中有6个峰 |
7.下列说法正确的是( )
| A. | 在标准状况下,1mol水和1molH2的体积都约是22.4L | |
| B. | 2gH2和44gCO2的体积相等 | |
| C. | 1mol某气体的体积为22.4L,则该气体一定处于标准状况 | |
| D. | 在标准状况下,1gH2和11.2LO2的物质的量相等 |
4.氯化铵是一种重要化工原料,也是一种常用的氨肥.
(1)氯化铵作为化肥时不宜与草木灰(主要成分K2CO3)混用.其原因是氯化铵与碳酸钾发生相互促进的水解反应生成氨气,会降低肥效.
(2)热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:6NH4++Fe2O3$\frac{\underline{\;加热\;}}{\;}$2Fe3++6NH3↑+3H2O.
(3)常温下,在20mLamol.L-1氨水中滴加加20mLbmol.L-1HCl溶液恰好至溶液呈中性.计算常温下,NH3.H2O的电离常数Kb=$\frac{a}{a-b}$×10-7mol/L(用含a,b的精确代数式表示)
(4)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
限选药品和仪器:恒温水浴、pH计、烧杯、0.1mol.L-1硝酸银溶液、蒸馏水和各种浓度的NH4Cl溶液.
①实验中,“待测物理量”是溶液的pH.
②i=30;ii:探究温度对氯化铵水解平衡的影响.
③上述表格中,y>(填“>”“<”或“=”)m.
(1)氯化铵作为化肥时不宜与草木灰(主要成分K2CO3)混用.其原因是氯化铵与碳酸钾发生相互促进的水解反应生成氨气,会降低肥效.
(2)热的浓氯化铵溶液可以清洗铁器表面锈迹,写出相关反应的离子方程式:6NH4++Fe2O3$\frac{\underline{\;加热\;}}{\;}$2Fe3++6NH3↑+3H2O.
(3)常温下,在20mLamol.L-1氨水中滴加加20mLbmol.L-1HCl溶液恰好至溶液呈中性.计算常温下,NH3.H2O的电离常数Kb=$\frac{a}{a-b}$×10-7mol/L(用含a,b的精确代数式表示)
(4)为了探究外界条件对氯化铵水解平衡的影响,设计如下实验方案:
| 实验序号 | c(NH4Cl)/mol.L-1 | 温度/℃ | 待测物理量 | 实验目的 |
| Ⅰ | 0.5 | 30 | x | - |
| Ⅱ | 1.5 | i | y | 探究浓度对氯化铵水解平衡的影响 |
| Ⅲ | 0.5 | 35 | z | ii |
| Ⅳ | 2.0 | 40 | m | 探究温度、浓度同时对氯化铵水解平衡的影响 |
①实验中,“待测物理量”是溶液的pH.
②i=30;ii:探究温度对氯化铵水解平衡的影响.
③上述表格中,y>(填“>”“<”或“=”)m.
18.在一容积为2L的恒容密闭容器中加入0.2mol CO和0.4mol H2,发生如下反应:CO(g)+2H2(g)?CH3OH(g).实验测得,300℃下,CH3OH的物质的量随时间的变化如下表所示.
(1)20min内,v(CH3OH)=0.003mol/(L•min).
(2)该温度下反应的化学平衡常数数值为2.25×104 .
(3)H2的平衡转化率是90%.
(4)若实验测得500℃下,到达平衡时n(CH3OH)=0.160mol,则正反应是放热(填“放热”或“吸热”)反应.
| t/min | 10 | 20 | 30 | 40 | 50 | 60 |
| n(CH3OH)/mol | 0.080 | 0.120 | 0.150 | 0.168 | 0.180 | 0.180 |
(2)该温度下反应的化学平衡常数数值为2.25×104 .
(3)H2的平衡转化率是90%.
(4)若实验测得500℃下,到达平衡时n(CH3OH)=0.160mol,则正反应是放热(填“放热”或“吸热”)反应.
19.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,1mol丙烷共用电子对数为6NA | |
| B. | 1mol甲醛与足量新制Cu(OH)2悬浊液反应,转移电子数目为2NA | |
| C. | 标准状况下,1L辛烷充分燃烧后生成气态产物的分子数为$\frac{8}{22.4}$NA | |
| D. | 0.1mol甲烷和0.1mol乙酸完全燃烧消耗的O2分子数都为0.2 NA |
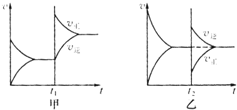 在一定条件下,有反应xA+yB?zC.
在一定条件下,有反应xA+yB?zC.