题目内容
关节炎的病因是在关节滑液中形成尿酸钠晶体(NaUr),尤其在寒冷季节易诱发关节疼痛,其化学机理为: (1)HUr+H2O?Ur-+H3O+ (2)Ur-+Na+?NaUr(s)
下列对反应(2)叙述:①正反应为吸热反应 ②正反应为放热反应 ③升高温度平衡向正反应方向移动 ④降低温度平衡向正反应方向移动. 其中正确的是( )
下列对反应(2)叙述:①正反应为吸热反应 ②正反应为放热反应 ③升高温度平衡向正反应方向移动 ④降低温度平衡向正反应方向移动. 其中正确的是( )
| A、①③ | B、②③ | C、①④ | D、②④ |
考点:吸热反应和放热反应,化学平衡的影响因素
专题:化学反应中的能量变化,化学平衡专题
分析:在寒冷季节易诱发关节疼痛,可见降低温度能促进尿酸钠晶体的形成,故反应(2)为放热反应,从而得出结论.
解答:
解:在寒冷季节易诱发关节疼痛,可见降低温度能促进尿酸钠晶体的形成,即温度降低,反应(2)平衡右移,故反应(2)正反应为放热反应,
①正反应放热,故①错误;
②正反应放热,故②正确;
③由于正反应放热,故升高温度平衡向逆反应方向移动. 故③错误;
④由于正反应放热,故降低温度平衡向正反应方向移动,故④正确.
故选D.
①正反应放热,故①错误;
②正反应放热,故②正确;
③由于正反应放热,故升高温度平衡向逆反应方向移动. 故③错误;
④由于正反应放热,故降低温度平衡向正反应方向移动,故④正确.
故选D.
点评:本题考查了温度的改变引起的平衡的移动,难度不大.

练习册系列答案
相关题目
据报道,科学家正在研究用容量更大的锌电池取代铅蓄电池,其电池反应式为2Zn+O2═2ZnO,原料是锌料、电解质溶液、空气.下列叙述中正确的是( )
| A、Zn是电池的正极 |
| B、负极反应:Zn-2e--═Zn2+ |
| C、正极发生氧化反应 |
| D、电解质溶液应选择稀硫酸 |
草酸是二元弱酸,草酸氢钾溶液呈酸性.在O.1mol?L-1 KHC2O4溶液中,下列关系正确的是( )
| A、c(HC2O4-)+c(C2O42-)=0.1mol?L-1 |
| B、c(C2O42-)>c(H2C2O4) |
| C、c(K+)=2c(H2C2O4)+2c(HC2O4- )+2c(C2O42-) |
| D、c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O4 2- ) |
在0.lmol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+对于该平衡,下列叙述正确的是( )
| A、加入少量NaOH固体,平衡向正向移动,溶液中c(H+)增大 |
| B、加水,平衡向正向移动,c(CH3COO- )和c(H+)增大 |
| C、通入少量 HCl,平衡逆向移动,溶液中c(H+)减少 |
| D、加入少量CH3COONa固体,平衡向逆向移动,溶液导电能力增强 |
下列物质中,不与盐酸反应,但可与氢氧化钠溶液反应的是( )
| A、Al(OH)3 |
| B、Al2O3 |
| C、SiO2 |
| D、Al |
NH3是一种重要的化工原料,可以制备一系列物质(如图).下列有关表述错误的是( )

| A、NH4Cl和NH4HCO3都是常用的化肥 |
| B、NH4Cl、HNO3和NaHCO3受热时都易分解 |
| C、图中所涉及的盐类物质均可以水解 |
| D、NH3和NO2在一定条件下可发生氧化还原反应 |
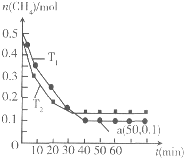 工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )| A、T1>T2 |
| B、b>0 |
| C、K(T1)>K(T2) |
| D、a点时NO2的转化率为33.3% |
中国科学院在世界上首次发现铂元素的一种同位素
Pt,它的中子数为( )
202 78 |
| A、78 | B、124 |
| C、202 | D、280 |
下列离子方程式正确的是( )
| A、氯水与水反应 Cl2+H2O=2H++Cl-+ClO- |
| B、铜与稀硫酸反应 Cu+2H+=Cu2++H2↑ |
| C、实验室制备氢氧化铝Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| D、向饱和碳酸钠溶液中滴加少量盐酸 CO32-+2H+=CO2↑+H2O |