题目内容
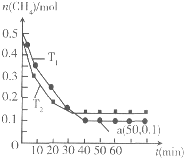 工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )
工业上消除氮氧化物的污染,可用如下反应:CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,测得n(CH4)随时间变化如图.下列说法正确的是( )| A、T1>T2 |
| B、b>0 |
| C、K(T1)>K(T2) |
| D、a点时NO2的转化率为33.3% |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:分析图象可知先拐先平温度高,T2>T1,温度越高甲烷物质的量减小,说明平衡正向进行,正反应为吸热反应,焓变大于0,平衡常数T2大于T1,a点位甲烷平衡物质的量为0.1mol,依据化学平衡三段式列式计算二氧化氮转化率;
解答:
解:A、分析图象可知先拐先平温度高,T2>T1,故A错误;
B、T2>T1,温度越高平衡时甲烷物质的量增大,说明平衡逆向进行,正反应为放热反应,焓变小于0,b<0,故B错误,
C、T2>T1,温度越高平衡时甲烷物质的量增大,说明平衡逆向进行,正反应为放热反应平衡常数T2小于T1,K(T1)>K(T2),故C正确;
D、平衡常数T2大于T1,a点位甲烷平衡物质的量为0.1mol,依据化学平衡三段式列式计算二氧化氮转化率,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,依据平衡三段式列式计算,设二氧化氮消耗量为x
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,
起始量(mol) 0.50 1.2 0 0 0
变化量(mol) 0.5 x x 0.5x 0.5x x
平衡量(mol)0.5-0.5x 1.2-x 0.5x 0.5x x
0.5-0.5x=0.1,x=0.8
二氧化氮转化率=
×100%=66.6%;故D错误;
故选C.
B、T2>T1,温度越高平衡时甲烷物质的量增大,说明平衡逆向进行,正反应为放热反应,焓变小于0,b<0,故B错误,
C、T2>T1,温度越高平衡时甲烷物质的量增大,说明平衡逆向进行,正反应为放热反应平衡常数T2小于T1,K(T1)>K(T2),故C正确;
D、平衡常数T2大于T1,a点位甲烷平衡物质的量为0.1mol,依据化学平衡三段式列式计算二氧化氮转化率,在温度T1和T2时,分别将0.50mol CH4和1.2mol NO2充入体积为1L的密闭容器中,依据平衡三段式列式计算,设二氧化氮消耗量为x
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g)△H=b kJ/mol,
起始量(mol) 0.50 1.2 0 0 0
变化量(mol) 0.5 x x 0.5x 0.5x x
平衡量(mol)0.5-0.5x 1.2-x 0.5x 0.5x x
0.5-0.5x=0.1,x=0.8
二氧化氮转化率=
| 0.8mol |
| 1.2mol |
故选C.
点评:本题考查了化学平衡图象分析判断,平衡影响因素分析和平衡移动原理的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
常温常压下,amL三种气态烃以任意比混合后,和足量O2混合点燃,恢复到原状态后,测得气体体积共缩小2a mL(不考虑CO2的溶解).则三种烃可能的组合( )
| A、C2H4、CH4、C3H4 |
| B、CH4、C3H6、C2H2 |
| C、C2H6、C3H6、C4H6 |
| D、C3H8、C4H8、C4H6 |
设NA为阿伏加德罗常数,下列说法中正确的是( )
| A、1mol Na2SO4溶于水中,所得溶液中Na+个数为NA |
| B、常温常压下24g 金属镁变成Mg2+失去电子2NA |
| C、标准状况下,22.4LH2O含有氢原子个数为2NA |
| D、11.2L氢气一定含有NA 个氢原子 |
 pH=2的X、Y、Z三种酸的溶液各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法错误的是( )
pH=2的X、Y、Z三种酸的溶液各1mL,分别加水稀释到1 000mL,其pH与溶液体积(V)的变化关系如图所示,下列说法错误的是( )| A、X是强酸,Y和Z是弱酸 |
| B、稀释前的浓度大小为c(Z)>c(Y)>c(X) |
| C、稀释前电离程度大小为X>Y>Z |
| D、pH=2时,X、Y、Z都是稀溶液 |
两种元素可以形成AB2型共价化合物的是( )
| A、无中子的原子与最外层有6个电子的短周期元素的原子 |
| B、核电荷数分别为12和17的元素 |
| C、ⅣA族和ⅥA族原子半径最小的元素 |
| D、最高正价都为奇数的两种短周期元素 |
取10.4g某醇与冰醋酸进行酯化反应,生成11.6g的酯,同时回收到未反应的醇3g,则醇可能是( )
| A、乙醇 | B、丁醇 | C、苯甲醇 | D、辛醇 |
下列说法中正确的是( )
| A、烃是指只含有碳、氢元素的有机物 |
| B、燃烧后能产生CO2和H2O的有机物一定是烃 |
| C、天然气、沼气、坑气、煤气的主要成分都是甲烷 |
| D、形成化合物种类最多的元素位于周期表中第二周期第VA族 |
下列各组中的性质比较,正确的是( )
| A、酸性HClO4>HBrO4>HIO4 |
| B、碱性NaOH>Mg(OH)2>Ca(OH)2 |
| C、C、N、O、F的最高正价依次升高 |
| D、氧化性:Na+>Mg2+>Al3+ |