题目内容
10.烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系: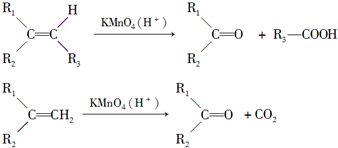
已知某烯烃的化学式为C4H8,它与酸性高锰酸钾溶液反应后得到的产物若为两个乙酸分子,则此烯烃的结构简式是CH3-CH=CH-CH3;若为二氧化碳和丙酮,则此烯烃的结构简式是CH3-C(CH3)=CH2.
分析 烯烃氧化规律可知,碳碳双键上碳原子连接一个氢原子,被高锰酸钾溶液氧化为羧基,碳碳双键的碳原子上连接两个氢原子被氧化为二氧化碳,若双键碳无氢原子连接则被氧化为羰基,据此分析结构简式.
解答 解:某烯烃的化学式为C4H8,它与酸性高锰酸钾溶液反应后得到的产物若为两个乙酸分子,则烯烃的结构简式是:CH3-CH=CH-CH3,若为二氧化碳和丙酮,则此烯烃的结构简式是:CH3-C(CH3)=CH2,
故答案为:CH3-CH=CH-CH3 ;CH3-C(CH3)=CH2.
点评 本题是给信息题,解题关键是看清烯烃与高锰酸钾酸性溶液反应的氧化产物的规律,题目难度中等.

练习册系列答案
相关题目
17.三氟化氮(NF3)是无色无味气体,它可由氟与氨直接反应得到:4NH3+3F2═NF3+3NH4F,下列叙述中正确的是( )
| A. | 在NF3中N的价态为-3价 | |
| B. | 该反应中NH3为还原剂,还原产物只有NF3 | |
| C. | 若有4 mol的氨气反应,转移的电子数目为6 NA | |
| D. | F2的摩尔质量为38 g |
15.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 18gH2O含有10NA个质子 | |
| C. | 2L 0.5mol/L 硫酸钾溶液中阴离子所含电荷数为NA | |
| D. | 准状况下,22.4LN2和H2混合气体中含NA个原子 |
5.阅读下面信息,推断元素,按要求回答问题:
| 信息 | 问题 |
| ①短周期元素X、Y、Z、W,原子序数依次增大,最外层电子数均不少于最内层电子数 | (1)X一定不是AD A.氢 B.碳 C.氧 D.硫 |
| ②一定条件下,上述四种元素的单质均能与足量的氧气反应,生成的氧化物有两种能溶于稀硫酸,三种能溶于浓NaOH溶液,氧化物的相对分子质量都大于26 | (2)这四种元素中有铝元素吗?可能 |
| ③向上述四种元素的单质的混合物中,加入足量的盐酸,固体部分溶解,过滤,向滤液中加入过量的烧碱溶液,最终溶液中有白色沉淀 | (3)白色沉淀的化学式为Mg(OH)2 |
| ④向上述四种元素的单质的混合物中,加入足量的烧碱溶液,固体部分溶解,过滤,向滤液中加入过量的盐酸,最终溶液中有白色沉淀 | (4)生成白色沉淀的离子方程式为SiO32-+2H+=H2SiO3↓(或SiO32-+2H++H2O=H4SiO4↓) |
| ⑤X与W同主族 | (5)X的最高价氧化物的电子式为 |
20.NA表示阿佛加德罗常数的值,下列叙述正确的是( )
| A. | 11.2L氯气中含有的原子数为NA个 | |
| B. | 标准状况下1mol苯的体积是22.4L | |
| C. | 1mol金属钠和足量的氧气反应生成过氧化钠可转移的电子数为NA | |
| D. | 1L1mol/L的硫酸钾溶液中,硫酸根和钾离子总数为2 N A |
 +Br2→
+Br2→
 .
.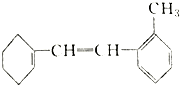 有机物M的结构简式如图所示.
有机物M的结构简式如图所示.