题目内容
15.某含苯环的烃A,其相对分子质量为104,碳的质量分数为92.3%.(1)A的分子式为C8H8.
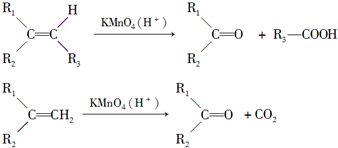
(2)A与溴的四氯化碳溶液反应的化学方程式为
 +Br2→
+Br2→
(3)在一定条件下,由A聚合得到的高分子化合物的结构简式为
 .
.
分析 1molA中n(C)=$\frac{104g×92.3%}{12g/mol}$=8mol,n(H)=$\frac{104g×(1-92.3%)}{1g/mol}$=8,则分子式为C8H8,A与溴的四氯化碳溶液反应,说明含有碳碳双键,则A为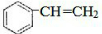 ,可发生加聚反应生成
,可发生加聚反应生成 ,以此解答该题.
,以此解答该题.
解答 解:(1)1molA中n(C)=$\frac{104g×92.3%}{12g/mol}$=8mol,n(H)=$\frac{104g×(1-92.3%)}{1g/mol}$=8,则分子式为C8H8,故答案为:C8H8;
(2)该物质含有苯环,能与溴发生反应,说明A应为苯乙烯,结构为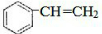 ,与溴发生加成反应生成
,与溴发生加成反应生成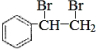 ,则反应的方程式为
,则反应的方程式为 +Br2→
+Br2→ ,
,
故答案为: +Br2→
+Br2→ ;
;
(3)含有C=C,可发生加聚反应生成聚苯乙烯,即 ,故答案为:
,故答案为: .
.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析、计算能力的考查,题目难度中等,注意根据元素的含量和相对分子质量推断A为解答该题的关键,学习中注意有机物官能团的性质.

练习册系列答案
相关题目
2.元素M的最高正价和负价的绝对值之差为6,M、N的离子具有相同的电子排布,则M、N所形成的化合物可能是( )
| A. | CaBr2 | B. | CaCl2 | C. | MgCl2 | D. | MgF2 |
3.某化合物6.4g在氧气中完全燃烧,只生成8.8gCO2和5.4gH2O.下列说法正确的是( )
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中一定含有氧元素 | ||
| C. | 该化合物中碳、氢原子个数比为1:2 | D. | 该有机物的分子式为C2H6 |
7.燃料电池是燃料(如CO、H2、CH4等)跟氧气(或空气)起反应将化学能转变为电能的装置,若电解质溶液是强碱溶液,下面关于甲烷燃料电池的说法正确的是( )
| A. | 负极反应式:O2+2H2O+4e-═4OH- | |
| B. | 负极反应式:CH4+8OH--8e-═CO2+6H2O | |
| C. | 随着放电的进行,溶液中的氢氧根离子浓度不变 | |
| D. | 放电时溶液中的阴离子向负极移动 |
5.用分液漏斗可以分离的一组混合物是( )
| A. | 碘和乙醇 | B. | 溴苯和水 | C. | 甲醇和乙二醇 | D. | 甘油和水 |