题目内容
17.三氟化氮(NF3)是无色无味气体,它可由氟与氨直接反应得到:4NH3+3F2═NF3+3NH4F,下列叙述中正确的是( )| A. | 在NF3中N的价态为-3价 | |
| B. | 该反应中NH3为还原剂,还原产物只有NF3 | |
| C. | 若有4 mol的氨气反应,转移的电子数目为6 NA | |
| D. | F2的摩尔质量为38 g |
分析 4NH3+3F2=NF3+3NH4F,该反应中NH3→NF3氮元素的化合价由-3价→+3价,一个氮气分子失去6个电子,所以氨气作还原剂被氧化;F2→F-氟元素得电子化合价降低,由0价→-1价,一个氟气分子得2个电子,氟气作氧化剂被还原,得失电子最小公倍数是6,所以氧化剂与还原剂的物质的量之比为3:1,结合元素化合价的变化与得失电子的关系解答.
解答 解:A、在NF3中F元素是-1价,所以N的价态为+3价,故A错误;
B、该反应中NH3为还原剂,还原产物有NF3和NH4F,故B错误;
C、由反应方程式:4NH3+3F2═NF3+3NH4F,若有4 mol的氨气反应,只有1mol的氨发生氧化反应,转移的电子数目为6 NA,故C正确;
D、摩尔质量的单位是g/mol,故D错误;
故选C.
点评 本题考查氧化还原反应,为高考常见题型,把握反应中元素的化合价变化为解答的关键,题目难度不大.

练习册系列答案
相关题目
7.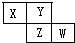 X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
 X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )
X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是( )| A. | Z元素的氧化物对应的水化物是强酸 | |
| B. | 含有X、Y、Z的化合物一定是共价化合物 | |
| C. | X的气态氢化物与W的气态氢化物反应的生成物中一定含有离子 | |
| D. | 原子半径大小顺序:X>Y>Z>W |
8.m mol C2H2跟n mol H2在密闭容器中反应,当该可逆反应达到平衡时,生成p mol C2H4.将反应后的混合气体完全燃烧生成CO2和H2O,所需要氧气的物质的量是( )
| A. | (3m+n)mol | B. | ($\frac{5}{2}$m+$\frac{n}{2}$-3p)mol | C. | (3m+n+2p)mol | D. | ($\frac{5}{2}$m+$\frac{n}{2}$)mol |
5.HgCl2的稀溶液可用作手术刀的消毒剂,已知HgCl2的熔点是2770C,熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力,则下列关于的叙述正确的是( )
| A. | HgCl2 属于共价化合物 | B. | HgCl2 属于离子化合物 | ||
| C. | HgCl2 属于非电解质 | D. | HgCl2属于强电解质 |
12.下列各组物质中,属于同分异构体的是( )
| A. | 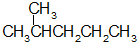 和 和 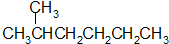 | |
| B. | H2N-CH2-COOH 和 H3C-CH2-NO2 | |
| C. | CH3-CH2-CH2-COOH 和 H3C-CH2-CH2-CH2-COOH | |
| D. | H3C-CH2-O-CH2-CH3和 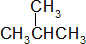 |
2.元素M的最高正价和负价的绝对值之差为6,M、N的离子具有相同的电子排布,则M、N所形成的化合物可能是( )
| A. | CaBr2 | B. | CaCl2 | C. | MgCl2 | D. | MgF2 |
6.化学反应前后一定发生变化的是( )
| A. | 原子个数 | B. | 化学键 | C. | 质量 | D. | 元素种类 |
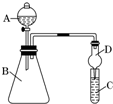 某同学利用如图装置来验证同主族元素非金属性的变化规律.
某同学利用如图装置来验证同主族元素非金属性的变化规律.