题目内容
卤素单质及其化合物在生产和生活中有广泛应用.
Ⅰ、氟化钠主要用作农作物杀菌剂、杀虫剂、木材防腐剂.实验室以氟硅酸(H2SiF6)等物质为原料、通过如下所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:
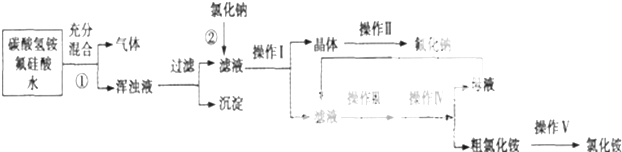
已知:20℃时氯化铵的溶解度为37.2g,氟化钠的溶解度为4g,Na2SiF6微溶于水.
请回答下列有关问题:
(1)完成并配平上述流程中①、②的化学反应方程式:
① H2SiF6+ NH4HCO3═ NH4F+ H2SiO3↓+ CO2↑+ ;
② .
(2)操作Ⅲ分为两步,其顺序是 (填写所选序号).
a、过滤 b、加热浓缩 c、冷却结晶 d、洗涤
操作Ⅱ是洗涤、干燥,其目的是 ,在操作Ⅰ~V中与之相同的操作步骤是 .
(3)流程①中NH4HCO3必须过量,其原因是 .
Ⅱ、紫菜与海带类似,是一种富含生物碘的海洋植物,可用于食用补碘.以下为某兴趣小组模拟从紫菜中提取碘的过程:
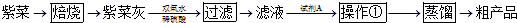
已知:商品紫菜轻薄松脆,比海带更易被焙烧成灰(此时碘转化为碘化物无机盐).
(4)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式: .
(5)操作①中涉及两步操作,名称是 ,所用的主要玻璃仪器为 ,所用试剂A最好选用表格中的 (填试剂名称).
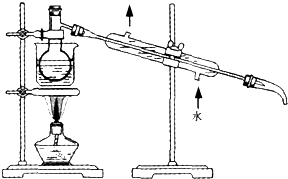
(6)将下列装置图中缺少的必要仪器补画出来,以最终将单质碘与试剂A分离:
Ⅰ、氟化钠主要用作农作物杀菌剂、杀虫剂、木材防腐剂.实验室以氟硅酸(H2SiF6)等物质为原料、通过如下所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:

已知:20℃时氯化铵的溶解度为37.2g,氟化钠的溶解度为4g,Na2SiF6微溶于水.
请回答下列有关问题:
(1)完成并配平上述流程中①、②的化学反应方程式:
①
②
(2)操作Ⅲ分为两步,其顺序是
a、过滤 b、加热浓缩 c、冷却结晶 d、洗涤
操作Ⅱ是洗涤、干燥,其目的是
(3)流程①中NH4HCO3必须过量,其原因是
Ⅱ、紫菜与海带类似,是一种富含生物碘的海洋植物,可用于食用补碘.以下为某兴趣小组模拟从紫菜中提取碘的过程:
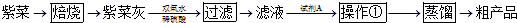
已知:商品紫菜轻薄松脆,比海带更易被焙烧成灰(此时碘转化为碘化物无机盐).
(4)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式:
(5)操作①中涉及两步操作,名称是
| 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) | |
| 密度/g、cm-3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |

考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:根据已知反应物和生成物,结合工艺流程可知,反应①为H2SiF6与NH4HCO3反应,生成的无味气体为CO2,过滤硅酸浑浊液,向滤液加入氯化钠,经过系列操作可得氟化钠、氯化铵,故滤液中含有氟化铵,故反应①为H2SiF66与NH4HCO3反应,生成CO2、硅酸、氟化铵,根据元素守恒还有水生成;反应②加入的反应物为NaCl,NaF比NaCl的溶解性小,是将第一步生成的NH4F转化为NaF;
(1)根据已知反应物和生成物,结合工艺流程可知,反应①为H2SiF6与NH4HCO3反应,生成的无味气体为CO2,过滤硅酸浑浊液,向滤液加入氯化钠,经过系列操作可得氟化钠、氯化铵,故滤液中含有氟化铵,故反应①为H2SiF66与NH4HCO3反应,生成CO2、硅酸、氟化铵,根据元素守恒还有水生成;
反应②加入的反应物为NaCl,NaF比NaCl的溶解性小,是将第一步生成的NH4F转化为NaF;
(2)加入的反应物为NaCl,NaF比NaCl的溶解性小,利用了物质在溶液中溶解度越小则优先析出的特性.操作Ⅰ是把固体与液体分离操作,应是过滤操作;操作II是将粗NaF洗涤除去其表面的杂质;操作Ⅲ是将滤液中的溶质进一步提取,应加热蒸发溶剂,析出大量固体后冷却,应是结晶;操作IV进行粗氯化铵提纯,应是重结晶;
(3)由信息可知,Na2SiF6微溶于水,流程中NH4HCO3必须过量,是指第一步操作中必须保证H2SiF6能全部反应,以防止反应②生成Na2SiF6;
(4)焙烧所得的紫菜灰主要含有碘离子,与足量的双氧水和稀硫酸作用,会发生氧化还原反应,方程式为:2I-+H2O2+2H+=I2+2H2O.
(5)操作①主要是将浸泡后紫菜灰和溶液的混合物中杂质去除,留下含碘离子的溶液,操作②主要是把碘单质从水中萃取到四氯化碳溶液中.
(6)为了实现实验目的,图2框图中缺少温度计和接受液体的装置及石棉网.
(1)根据已知反应物和生成物,结合工艺流程可知,反应①为H2SiF6与NH4HCO3反应,生成的无味气体为CO2,过滤硅酸浑浊液,向滤液加入氯化钠,经过系列操作可得氟化钠、氯化铵,故滤液中含有氟化铵,故反应①为H2SiF66与NH4HCO3反应,生成CO2、硅酸、氟化铵,根据元素守恒还有水生成;
反应②加入的反应物为NaCl,NaF比NaCl的溶解性小,是将第一步生成的NH4F转化为NaF;
(2)加入的反应物为NaCl,NaF比NaCl的溶解性小,利用了物质在溶液中溶解度越小则优先析出的特性.操作Ⅰ是把固体与液体分离操作,应是过滤操作;操作II是将粗NaF洗涤除去其表面的杂质;操作Ⅲ是将滤液中的溶质进一步提取,应加热蒸发溶剂,析出大量固体后冷却,应是结晶;操作IV进行粗氯化铵提纯,应是重结晶;
(3)由信息可知,Na2SiF6微溶于水,流程中NH4HCO3必须过量,是指第一步操作中必须保证H2SiF6能全部反应,以防止反应②生成Na2SiF6;
(4)焙烧所得的紫菜灰主要含有碘离子,与足量的双氧水和稀硫酸作用,会发生氧化还原反应,方程式为:2I-+H2O2+2H+=I2+2H2O.
(5)操作①主要是将浸泡后紫菜灰和溶液的混合物中杂质去除,留下含碘离子的溶液,操作②主要是把碘单质从水中萃取到四氯化碳溶液中.
(6)为了实现实验目的,图2框图中缺少温度计和接受液体的装置及石棉网.
解答:
解:(1)反应①为H2SiF66与NH4HCO3反应,生成CO2、硅酸、氟化铵、水,依据原子守恒配平书写得到反应方程式为:
H2SiF6+6NH4HCO3═6NH4F+H2SiO3↓+6CO2↑+3H2O;
反应②是将第一步生成的NH4F转化为NaF,反应方程式为:NH4F+NaCl═NaF↓+NH4Cl,
故答案为:1,6,6,1,6,3H2O;NH4F+NaCl═NaF↓+NH4Cl;
(2)操作Ⅰ是把固体与液体分离操作,应是过滤操作;
操作II是将粗NaF洗涤除去其表面的杂质,操作为:待母液全部滤出后,再向滤纸上加蒸馏水至恰好浸没晶体,静置让其滤出,重复操作2-3次,以除去晶体表面的杂质;
操作Ⅲ是将滤液中的溶质进一步提取,应加热蒸发溶剂,析出大量固体后冷却,应是结晶;
操作IV进行粗氯化铵提纯,应是重结晶,
操作V进行粗氯化铵提纯,应是重结晶,
操作Ⅲ分为两步、加热浓缩,冷却结晶,故选bc;操作Ⅱ是洗涤、干燥,其目的是:除去氟化钠表面的氯化铵等可溶性杂质;在操作Ⅰ~V中与操作Ⅱ相同的操作步骤是除去杂质的实验操作,应是V;
故答案为:bc,除去氟化钠表面的氯化铵等可溶性杂质,V;
(3)流程中NH4HCO3必须过量,是指第一步操作中必须保证H2SiF6能全部反应,防止生成Na2SiF6沉淀,防止在进行反应②H2SiF6将与NaCl反应,生成Na2SiF6沉淀,混入NaF中影响NaF质量,
故答案为:保证H2SiF6能全部反应,防止生成Na2SiF6沉淀,混入NaF中影响NaF质量.
(4)焙烧所得的紫菜灰主要含有碘离子,与足量的双氧水和稀硫酸作用,会发生氧化还原反应,方程式为:2I-+H2O2+2H+=I2+2H2O;
故答案为:2I-+H2O2+2H+=I2+2H2O.
(5)将浸泡后紫菜灰和溶液的混合物中杂质去除,留下含碘离子的溶液,操作①主要是把碘单质从水中萃取到四氯化碳溶液中,然后再分液,且在分液时下层液体从下口放出后,上层液体要从上口倒出,萃取剂需要满足不溶于水,不能和碘单质反应,乙醇易溶于水不能分层,裂化汽油和碘单质发生反应,所以需要试剂A为四氯化碳;
故答案为:萃取分液;分液漏斗;四氯化碳.
(6)为了实现实验目的,图2框图中缺少温度计和接受液体的装置及石棉网,装置如图 :
:
故答案为: ;
;
H2SiF6+6NH4HCO3═6NH4F+H2SiO3↓+6CO2↑+3H2O;
反应②是将第一步生成的NH4F转化为NaF,反应方程式为:NH4F+NaCl═NaF↓+NH4Cl,
故答案为:1,6,6,1,6,3H2O;NH4F+NaCl═NaF↓+NH4Cl;
(2)操作Ⅰ是把固体与液体分离操作,应是过滤操作;
操作II是将粗NaF洗涤除去其表面的杂质,操作为:待母液全部滤出后,再向滤纸上加蒸馏水至恰好浸没晶体,静置让其滤出,重复操作2-3次,以除去晶体表面的杂质;
操作Ⅲ是将滤液中的溶质进一步提取,应加热蒸发溶剂,析出大量固体后冷却,应是结晶;
操作IV进行粗氯化铵提纯,应是重结晶,
操作V进行粗氯化铵提纯,应是重结晶,
操作Ⅲ分为两步、加热浓缩,冷却结晶,故选bc;操作Ⅱ是洗涤、干燥,其目的是:除去氟化钠表面的氯化铵等可溶性杂质;在操作Ⅰ~V中与操作Ⅱ相同的操作步骤是除去杂质的实验操作,应是V;
故答案为:bc,除去氟化钠表面的氯化铵等可溶性杂质,V;
(3)流程中NH4HCO3必须过量,是指第一步操作中必须保证H2SiF6能全部反应,防止生成Na2SiF6沉淀,防止在进行反应②H2SiF6将与NaCl反应,生成Na2SiF6沉淀,混入NaF中影响NaF质量,
故答案为:保证H2SiF6能全部反应,防止生成Na2SiF6沉淀,混入NaF中影响NaF质量.
(4)焙烧所得的紫菜灰主要含有碘离子,与足量的双氧水和稀硫酸作用,会发生氧化还原反应,方程式为:2I-+H2O2+2H+=I2+2H2O;
故答案为:2I-+H2O2+2H+=I2+2H2O.
(5)将浸泡后紫菜灰和溶液的混合物中杂质去除,留下含碘离子的溶液,操作①主要是把碘单质从水中萃取到四氯化碳溶液中,然后再分液,且在分液时下层液体从下口放出后,上层液体要从上口倒出,萃取剂需要满足不溶于水,不能和碘单质反应,乙醇易溶于水不能分层,裂化汽油和碘单质发生反应,所以需要试剂A为四氯化碳;
故答案为:萃取分液;分液漏斗;四氯化碳.
(6)为了实现实验目的,图2框图中缺少温度计和接受液体的装置及石棉网,装置如图
 :
:故答案为:
 ;
;
点评:本题主要考查了化学与工业生产的相关知识、阅读题目与工艺流程获取信息能力、物质的分离提纯、对实验操作的理解等,难度中等,理解工艺流程是解题关键,需要学生具备扎实的基础与综合运用信息分析问题、解决问题的能力.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
下列反应属于氧化还原反应的是( )
| A、CaO+H2O═Ca(OH)2 | ||||
B、Fe2O3+3CO
| ||||
C、CaCO3
| ||||
| D、CO2+2NaOH═Na2CO3+H2O |
下列化学用语表示正确的是( )
A、HCl的电子式: |
B、NH4Cl的电子式: |
C、CCl4的电子式: |
D、硫离子的结构示意图为 |
在酸性溶液中,可以大量共存的离子是( )
| A、Na+ K+ HCO3- Cl- |
| B、NH4+ Mg2+ SO42- Cl- |
| C、K+ Na+ SO42- CH3COO- |
| D、K+ Ca2+ CO32- NO3- |
下列物质中,属于纯净物的是( )
| A、生铁 | B、铝热剂 |
| C、磁铁矿 | D、绿矾 |


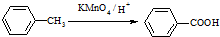
 (苯胺,易被氧化)
(苯胺,易被氧化)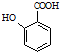 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物有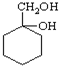 最合理的方案(不超过4步)
最合理的方案(不超过4步) .
.