题目内容
8.某有机物如图.下列说法错误的是( )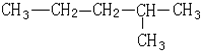
| A. | 该有机物属于烷烃 | |
| B. | 该烃与2,3-二甲基丁烷互为同系物 | |
| C. | 该烃的一氯取代产物共有5种 | |
| D. | 该有机物可由两种单炔烃分别与氢气加成得到 |
分析 该有机物为2-甲基戊烷,可由HC≡C-CH2CH(CH3)2、CH3C≡CCH(CH3)2与氢气发生加成反应生成,结合等效氢原子的数目解答该题.
解答 解:A.为饱和烃,属于烷烃,故A正确;
B.有机物为2-甲基戊烷,与2,3-二甲基丁烷互为同分异构体,故B错误;
C.分子中有5种位置不同的H原子,则一氯取代产物共有5种,故C正确;
D.可由HC≡C-CH2CH(CH3)2、CH3C≡CCH(CH3)2与氢气发生加成反应生成,故D正确.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重学生的分析能力的考查,题目难度不大,学习中注意有机物的官能团的结构和性质.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
16.短周期元素X、Y、Z、Q在元素周期表中的相对位置如图,地壳中含量最高的元素已包含其中.回答下列问题:
(1)Q在元素周期表中的位置是第二周期VIA族.X离子的结构示意图为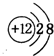 .
.
(2)下列选项中,能证明元素非金属性Z强于Y的是C.
A.反应中,Y原子得到的电子数比Z原子得到的电子数多
B.最高正价,Z比Y的高
C.最高价氧化物的水化物酸性:Z>Y
(3)ZQ2是国际公认高效安全杀菌消毒剂,已知ZQ2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ZQ2被还原为Z-,该反应的离子方程式为5Mn2++2ClO2+6H2O=5MnO2↓+2Cl-+12H+.
(4)H元素与Y形成的化合物中二者的质量之比是1:3,已知常温下4g该化合物完全燃烧并恢复到原来温度时放出222.6kJ热量,则表示该化合物燃烧热的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.4kJ/mol.
(5)表中X的最高价氧化物对应水化物的化学式为X(OH)n,在25℃时,其饱和溶液能使酚酞试液变红,则其饱和溶液中的pH=10.3(已知:25℃,Ksp[X(OH)n]=4.0×l0-12;lg5=0.7).
| Y | Q | ||||
| X | Z |
 .
.(2)下列选项中,能证明元素非金属性Z强于Y的是C.
A.反应中,Y原子得到的电子数比Z原子得到的电子数多
B.最高正价,Z比Y的高
C.最高价氧化物的水化物酸性:Z>Y
(3)ZQ2是国际公认高效安全杀菌消毒剂,已知ZQ2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ZQ2被还原为Z-,该反应的离子方程式为5Mn2++2ClO2+6H2O=5MnO2↓+2Cl-+12H+.
(4)H元素与Y形成的化合物中二者的质量之比是1:3,已知常温下4g该化合物完全燃烧并恢复到原来温度时放出222.6kJ热量,则表示该化合物燃烧热的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.4kJ/mol.
(5)表中X的最高价氧化物对应水化物的化学式为X(OH)n,在25℃时,其饱和溶液能使酚酞试液变红,则其饱和溶液中的pH=10.3(已知:25℃,Ksp[X(OH)n]=4.0×l0-12;lg5=0.7).
3.下列有关化学实验的叙述中,不正确的是( )
| A. | 用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率 | |
| B. | 蒸馏时应调整温度计的水银球于蒸馏烧瓶支管口附近 | |
| C. | 制备乙酸乙酯时,为除去乙酸乙酯中的乙酸,用氢氧化钠溶液收集产物 | |
| D. | 重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤 |
20.用NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 14 g氮气所含质子数目为7 NA | |
| B. | 7.8 g苯含有碳碳双键的数目为0.3NA | |
| C. | 标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.2NA | |
| D. | 1molNa2O2中离子总数是3NA |
17.下列叙述正确的是( )
| A. | 用惰性电极电解某溶液时,若两极分别只有H2和O2生成,电解一段时间后,该溶液的浓度可能减小 | |
| B. | 电解精炼铜时,电解质溶液中铜离子浓度可能减小 | |
| C. | 原电池工作时,溶液中的阳离子向负极移动 | |
| D. | 要使电解后的CuSO4溶液复原,可向其中加人Cu(OH)2固体 |
18.将ag Fe2O3、Al2O3样品溶解在过量的200mL 0.05mol/L的硫酸溶液中然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
| A. | 0.1 mol•L-1 | B. | 0.2 mol•L-1 | C. | 0.4 mol•L-1 | D. | 0.8 mol•L-1 |


 ;
;