题目内容
20.用NA表示阿伏加德罗常数的值,下列说法不正确的是( )| A. | 14 g氮气所含质子数目为7 NA | |
| B. | 7.8 g苯含有碳碳双键的数目为0.3NA | |
| C. | 标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.2NA | |
| D. | 1molNa2O2中离子总数是3NA |
分析 A.依据n=$\frac{m}{M}$计算物质的量,氮气分子中含质子数为14;
B.苯分子中无碳碳双键;
C.根据氯气和铁反应后变为-1价来分析;
D.过氧化钠是由1个过氧根离子和2个钠离子构成,所以其阴阳离子个数之比为1:2,据此计算离子总数.
解答 解:A.14 g氮气物质的量=$\frac{14g}{28g/mol}$=0.5mol,所含质子数目=0.5mol×14×NA=7 NA,故A正确;
B.苯分子中无碳碳双键,是六个碳碳键完全等同的特殊化学键,故B错误;
C.标况下,2.24L的氯气为0.1mol,而和铁反应后变为-1价,故0.1mol氯气转移0.2mol电子即0.2NA个,故C正确;
D.过氧化钠化学式是由1个过氧根离子和2个钠离子构成,所以其阴阳离子个数之比为1:2,则1molNa2O2固体中含有离子总数为3NA,故D正确;
故选B.
点评 本题考查了阿伏伽德罗常数、物质的量有关计算,掌握公式的运用以及物质的结构是解题关键,注意苯分子的结构,题目难度不大.

练习册系列答案
相关题目
9.洗涤盛放过植物油的试管,宜选用的试剂是( )
| A. | 稀硫酸 | B. | 热的碳酸钠溶液 | C. | 热水 | D. | 浓硝酸 |
8.某有机物如图.下列说法错误的是( )
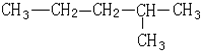
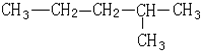
| A. | 该有机物属于烷烃 | |
| B. | 该烃与2,3-二甲基丁烷互为同系物 | |
| C. | 该烃的一氯取代产物共有5种 | |
| D. | 该有机物可由两种单炔烃分别与氢气加成得到 |
5.要想证明某溶液中是否含有Fe3+,下列操作中正确的是( )
| A. | 加入铁粉 | B. | 通入氯气 | C. | 加入铜片 | D. | 滴加KSCN溶液 |
9.下列化学用语表达不正确的是( )
| A. | 丙烷的球棍模型为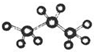 | B. | 丙烯的结构简式为CH3CHCH2 | ||
| C. | 符合通式CnH2n+2的一定是烷烃 | D. | O2、O3属于同素异形体 |
10.下列常见分子的中心原子的杂化轨道类型是SP3的是( )
| A. | NH4+ | B. | CH4 | C. | SO2 | D. | CO2 |
 ,并推测1mol NH4BF4(氟硼酸铵)中含有2NA个配位键.
,并推测1mol NH4BF4(氟硼酸铵)中含有2NA个配位键.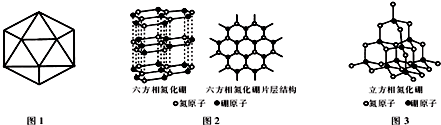
 .
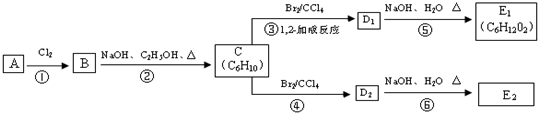
.
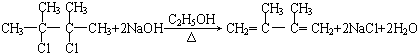 ,C的化学名称是2,3-二甲基-1,3-丁二烯,反应⑥的化学方程式为
,C的化学名称是2,3-二甲基-1,3-丁二烯,反应⑥的化学方程式为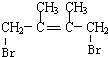 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$ +2NaBr,④的反应类型是加成反应.
+2NaBr,④的反应类型是加成反应.