题目内容
回答下列问题.
(1)碳酸氢钠可治疗胃酸过多,发生反应的离子方程式为 .
(2)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为 ;漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 .
(3)查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是 .
(1)碳酸氢钠可治疗胃酸过多,发生反应的离子方程式为
(2)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为
(3)查阅资料得知,铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等,向铝土矿中加入足量烧碱溶液后,发生反应的离子方程式是
考点:钠的重要化合物,氯气的化学性质,镁、铝的重要化合物
专题:元素及其化合物
分析:(1)碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳;
(2)石灰乳与氯气反应生成氯化钙、次氯酸钙和水;次氯酸的酸性比碳酸弱,次氯酸钙和与二氧化碳、水反应生成次氯酸;
(3)向铝土矿中加入足量烧碱溶液,氧化铝、二氧化硅都可与氢氧化钠反应.
(2)石灰乳与氯气反应生成氯化钙、次氯酸钙和水;次氯酸的酸性比碳酸弱,次氯酸钙和与二氧化碳、水反应生成次氯酸;
(3)向铝土矿中加入足量烧碱溶液,氧化铝、二氧化硅都可与氢氧化钠反应.
解答:
解:(1)碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,反应的离子方程式为HCO3-+H+=H2O+CO2↑,
故答案为:HCO3-+H+=H2O+CO2↑;
(2)石灰乳与氯气反应生成氯化钙、次氯酸钙和水,反应的方程式为2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;次氯酸的酸性比碳酸弱,次氯酸钙和与二氧化碳、水反应生成次氯酸,化学反应方程式为Ca(ClO)2+CO2+H2O═CaCO3↓+2 HClO,
故答案为:2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;
(3)向铝土矿中加入足量烧碱溶液,氧化铝、二氧化硅都可与氢氧化钠反应,反应的离子方程式分别为Al2O3+2OH-=2AlO2-+H2O、SiO2+2OH-=SiO32-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O、SiO2+2OH-=SiO32-+H2O.
故答案为:HCO3-+H+=H2O+CO2↑;
(2)石灰乳与氯气反应生成氯化钙、次氯酸钙和水,反应的方程式为2Cl2+2 Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;次氯酸的酸性比碳酸弱,次氯酸钙和与二氧化碳、水反应生成次氯酸,化学反应方程式为Ca(ClO)2+CO2+H2O═CaCO3↓+2 HClO,
故答案为:2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O;Ca(ClO)2+CO2+H2O═CaCO3↓+2HClO;
(3)向铝土矿中加入足量烧碱溶液,氧化铝、二氧化硅都可与氢氧化钠反应,反应的离子方程式分别为Al2O3+2OH-=2AlO2-+H2O、SiO2+2OH-=SiO32-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O、SiO2+2OH-=SiO32-+H2O.
点评:本题综合考查元素化合物知识,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意把握相关基础知识的积累,难度不大.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
实验操作的规范是实验的基本要求,下列实验操作正确的是( )
A、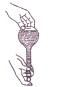 检验容量瓶是否漏水 |
B、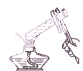 给溶液加热 |
C、 滴加液体 |
D、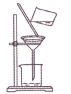 过滤 |
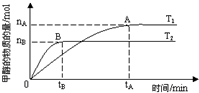 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ?mol-1、-283.0kJ?mol-1和-726.5kJ?mol-1.请回答下列问题: