��Ŀ����
A��B��C��D��E���Ƕ�����Ԫ�أ�ԭ�Ӱ뾶D��C��A��E��B������A��B����ͬһ���ڣ�A��C����ͬһ���壮Cԭ�Ӻ�������������A��Bԭ�Ӻ���������֮�ͣ�Cԭ��������ϵĵ�������Dԭ��������������4������DΪ�������Իش�
��1��C��Ԫ�����ڱ��ĵ� ���� �壮
��2��������Ԫ���У����γɵ����Һ̬����̬�⻯����ȶ����ɴ�С��˳���ǣ��þ���ķ���ʽ��ʾ�� ��
��3��A��B�γɵ���ԭ�ӷ��ӵĽṹʽ�� ��B��D�γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����ĵ���ʽ�� ��
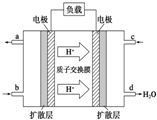
��4��E��һ���⻯����£��������Eԭ������ԭ�Ӹ�����Ϊ1��2����-����ȼ�ϵ����һ�ֻ�������ȼ�ϵ�أ���������Һ��20%-30%��KOH��Һ����ȼ�ϵ�ص������ĵ缫��Ӧʽ�� ��
��1��C��Ԫ�����ڱ��ĵ�
��2��������Ԫ���У����γɵ����Һ̬����̬�⻯����ȶ����ɴ�С��˳���ǣ��þ���ķ���ʽ��ʾ��
��3��A��B�γɵ���ԭ�ӷ��ӵĽṹʽ��
��4��E��һ���⻯����£��������Eԭ������ԭ�Ӹ�����Ϊ1��2����-����ȼ�ϵ����һ�ֻ�������ȼ�ϵ�أ���������Һ��20%-30%��KOH��Һ����ȼ�ϵ�ص������ĵ缫��Ӧʽ��
���㣺ԭ�ӽṹ��Ԫ�������ɵĹ�ϵ,��ѧ��Դ���͵��
ר�⣺Ԫ����������Ԫ�����ڱ�ר��,�绯ѧר��
������Cԭ��������ϵĵ�������Dԭ��������������4������DΪ������DӦΪ��A��Ԫ�أ�CΪ��A��Ԫ�أ�Dԭ�Ӱ뾶���ӦΪNaԪ�أ�A��C����ͬһ���壬��AΪCԪ�أ�CΪSiԪ�أ�Cԭ�Ӻ�������������A��Bԭ�Ӻ���������֮�ͣ�B��ԭ������Ϊ14-6=8����BΪOԪ�أ���ԭ�Ӱ뾶A��E��B��֪EӦΪNԪ�أ��Դ˽����⣮
���
�⣺Cԭ��������ϵĵ�������Dԭ��������������4������DΪ������DӦΪ��A��Ԫ�أ�CΪ��A��Ԫ�أ�Dԭ�Ӱ뾶���ӦΪNaԪ�أ�A��C����ͬһ���壬��AΪCԪ�أ�CΪSiԪ�أ�Cԭ�Ӻ�������������A��Bԭ�Ӻ���������֮�ͣ�B��ԭ������Ϊ14-6=8����BΪOԪ�أ���ԭ�Ӱ뾶A��E��B��֪EӦΪNԪ�أ�
��1�������Ϸ��ӿ�֪CΪSiԪ�أ�λ�����ڱ����������ڢ�AԪ�أ��ʴ�Ϊ��������A��
��2��������Ԫ���У����γɵ����Һ̬����̬�⻯����C��N��O��Si�ȣ���ǽ�����O��N��C��Si��Ԫ�صķǽ�����Խǿ�����Ӧ���⻯����ȶ���Խǿ���ȶ����ɴ�С��˳����H2O��NH3��CH4��SiH4��
�ʴ�Ϊ��H2O��NH3��CH4��SiH4��
��3��A��B�γɵ���ԭ�ӷ���ΪCO2��Ϊֱ���η��ӣ��ṹʽΪO=C=O��B��D�γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����Ϊ�������ƣ�����ʽΪ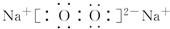 ��
��
�ʴ�Ϊ��O=C=O��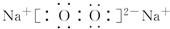 ��
��
��4��ȼ�ϵ�ص�����Ϊ�����õ��ӵĻ�ԭ��Ӧ���缫����ʽΪO2+2H2O+4e-=4OH-���ʴ�Ϊ��O2+2H2O+4e-=4OH-��
��1�������Ϸ��ӿ�֪CΪSiԪ�أ�λ�����ڱ����������ڢ�AԪ�أ��ʴ�Ϊ��������A��
��2��������Ԫ���У����γɵ����Һ̬����̬�⻯����C��N��O��Si�ȣ���ǽ�����O��N��C��Si��Ԫ�صķǽ�����Խǿ�����Ӧ���⻯����ȶ���Խǿ���ȶ����ɴ�С��˳����H2O��NH3��CH4��SiH4��
�ʴ�Ϊ��H2O��NH3��CH4��SiH4��
��3��A��B�γɵ���ԭ�ӷ���ΪCO2��Ϊֱ���η��ӣ��ṹʽΪO=C=O��B��D�γɵ�ԭ�Ӹ�����Ϊ1��1�Ļ�����Ϊ�������ƣ�����ʽΪ
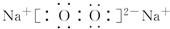 ��
���ʴ�Ϊ��O=C=O��
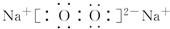 ��
����4��ȼ�ϵ�ص�����Ϊ�����õ��ӵĻ�ԭ��Ӧ���缫����ʽΪO2+2H2O+4e-=4OH-���ʴ�Ϊ��O2+2H2O+4e-=4OH-��
���������⿼��Ԫ��λ�ýṹ���ʵĹ�ϵ����Ŀ�Ѷ��еȣ��ؼ�����ȷ�ƶ�Ԫ�ص����࣬ע�����ԭ��λ�ù�ϵ���뾶��С�ҳ��������ڱ��е����λ�ã�

��ϰ��ϵ�д�
 ������ҵ��ͬ����ϰ��ϵ�д�
������ҵ��ͬ����ϰ��ϵ�д�
�����Ŀ
��������������ԭ����0.1mol H3PO4������ԭ����Ŀ��ȵ��ǣ�������
| A��0.2mol H2O2 |
| B��0.1mol H2SO4 |
| C��0.2mol NaOH |
| D��0.3mol H2O |
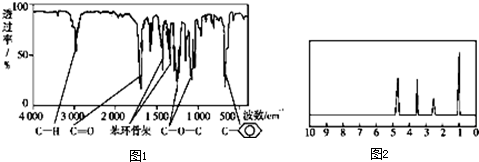
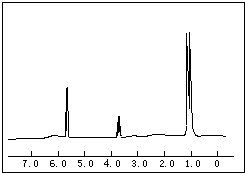 ��1�������л����������Ӧ������ ��CH3CH2CH3��CH2=CH-CH3��CH3COOCH3��H3C-OH��CH3CH2COOH ����
��1�������л����������Ӧ������ ��CH3CH2CH3��CH2=CH-CH3��CH3COOCH3��H3C-OH��CH3CH2COOH ����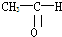 ϩ����
ϩ����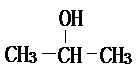 �е�һ�֣�����ͼ����Ϣ����ṹ��ʽΪ��
�е�һ�֣�����ͼ����Ϣ����ṹ��ʽΪ��