题目内容
18.下列各组混合物中,能用分液漏斗进行分离的是( )| A. | 碘和四氯化碳 | B. | 汽油和柴油 | C. | 水和四氯化碳 | D. | 水和醋酸 |
分析 能用分液漏斗进行分离,则混合物分层,结合物质的溶解性来解答.
解答 解:A、B、D中的物质互溶,不分层,不能利用分液漏斗进行分离,而C中水和四氯化碳互不相溶,出现分层,则能利用分液漏斗进行分离,
故选C.
点评 本题考查混合物的分离和提纯,为高频考点,把握物质的性质、性质差异、混合物分离方法为解答的关键,侧重于学生的分析能力和实验能力的考查,注意仪器的使用,题目难度不大.

练习册系列答案
相关题目
8.25℃时,将0.0lmol•L-1的盐酸与b mol•L-1的氨水等体积混合,反应后溶液呈中性(忽略溶液混合后体积的变化).下列说法不正确的是( )
| A. | 此时水的电离程度并不是最大 | |
| B. | 混合溶液中的离子浓度:c(NH4+)=c(Cl-)>c(H+)=c(OH-) | |
| C. | 此时溶液中NH3•H2O的浓度为$\frac{1}{2}$(b-0.01)mol.L-1 | |
| D. | 用含b的代数式不能表示25℃时NH3•H2O的电离常数 |
6.用NA表示阿伏伽德罗常数的值,下列叙述中正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 25℃、101kPa下,64g SO2中含有的原子数为3NA | |
| C. | 在常温常压下,11.2L Cl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
13.如图是元素周期表的一部分,下列说法正确的是( )
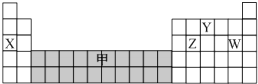

| A. | 离子半径:W->X+>Y3- | |
| B. | 可在灰色区域“甲”中寻找催化剂 | |
| C. | 气态氢化物的稳定性:Z>W | |
| D. | 工业上电解 X和 W化合物的水溶液制备 X |
3.下列实验操作与安全事故处理错误的是( )
| A. | 点燃乙烯气体前,必须先检验乙烯的纯度 | |
| B. | 过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 | |
| C. | 如果没有试管夹,可以临时手持试管给固体或液体加热 | |
| D. | 酒精灯洒出的酒精在桌上着火,应立即用湿抹布盖灭 |
10.下列反应属于取代反应的是( )
| A. | 乙烯和酸性高锰酸钾溶液的反应 | |
| B. | 在一定条件下,乙烯和水的反应 | |
| C. | 在FeBr3催化作用下,苯和溴的反应 | |
| D. | 在镍作催化剂、加热的条件下,苯和氢气的反应 |
7.下列排序不正确的是( )
| A. | 单质的熔点:钾<铷<铯 | B. | 离子半径:S2->Na+>Mg2+ | ||
| C. | 热稳定性:HF>H2O>H2S | D. | 酸性:H2SiO3<H3PO4<H2SO4 |
8.下列关于使用托盘天平的叙述不正确的是 ( )
| A. | 称量前先调节托盘天平的零点 | |
| B. | 称量时左盘放被称量物,右盘放砝码 | |
| C. | 潮湿的或具有腐蚀性的药品,必须放在玻璃器皿里称量.其他固体药品可直接放在天平托盘上称量 | |
| D. | 用托盘天平可以准确称量药品0.01g | |
| E. | 称量完毕应把砝码放回砝码盒中 |