题目内容
13.如图是元素周期表的一部分,下列说法正确的是( )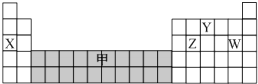
| A. | 离子半径:W->X+>Y3- | |
| B. | 可在灰色区域“甲”中寻找催化剂 | |
| C. | 气态氢化物的稳定性:Z>W | |
| D. | 工业上电解 X和 W化合物的水溶液制备 X |
分析 由元素的位置可知,X为Na,Y为N,Z为Si,W为Cl,
A.电子层越多,离子半径越大;具有相同电子排布的离子中原子序数大的离子半径小;
B.灰色区域“甲”均为金属元素;
C.非金属性越强,对应氢化物越稳定;
D.电解NaCl溶液生成NaOH、氢气、氯气.
解答 解:由元素的位置可知,X为Na,Y为N,Z为Si,W为Cl,
A.电子层越多,离子半径越大;具有相同电子排布的离子中原子序数大的离子半径小,则离子半径:W->Y3->X+,故A错误;
B.灰色区域“甲”均为金属元素,则可寻找催化剂,故B正确;
C.非金属性越强,对应氢化物越稳定,则气态氢化物的稳定性:W>Z,故C错误;
D.电解NaCl溶液生成NaOH、氢气、氯气,应电解熔融NaCl制备Na,故D错误;
故选B.
点评 本题考查位置、结构与性质的关系,为高频考点,把握元素的位置、元素周期律、元素化合物知识为解答的关键,侧重分析与应用能力的考查,注意Na的制备方法,题目难度不大.

练习册系列答案
相关题目
3. 表是元素周期表的前三周期:
表是元素周期表的前三周期:
回答下列问题:
(1)J元素的元素的名称:氩.
(2)G元素与I 元素形成的化合物的电子式是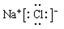 ,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是HClO4,属于两性氢氧化物的是Al(OH)3(用化合物的化学式表示).
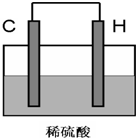
(4)将H单质与C的一种单质(导体)按如图装置连接,其中C极为正极(填正或负),并写出该电极反应式为:2H++2e-=H2↑.
 表是元素周期表的前三周期:
表是元素周期表的前三周期:| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 一 | A | |||||||
| 二 | B | C | D | E | F | |||
| 三 | G | H | I | J |
(1)J元素的元素的名称:氩.
(2)G元素与I 元素形成的化合物的电子式是
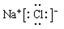 ,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.
,A、G、E形成的化合物中含有的化学键类型为离子键、共价键.(3)表格中十种元素的最高氧化物对应的水化物中,酸性最强的是HClO4,属于两性氢氧化物的是Al(OH)3(用化合物的化学式表示).
(4)将H单质与C的一种单质(导体)按如图装置连接,其中C极为正极(填正或负),并写出该电极反应式为:2H++2e-=H2↑.
1.下列除去杂质的方法正确的是( )
①除去乙醇中少量的乙醛:加入新制的氢氧化铜浊液,加热至沸腾,过滤取溶液
②除去福尔马林中少量的蚁酸:加入足量饱和碳酸钠溶液,充分振荡、蒸馏,收集馏出物
③除去苯中少量的苯酚:加溴水,振荡,过滤除去沉淀
④除去乙醇中少量的水:加足量新制生石灰,蒸馏.
①除去乙醇中少量的乙醛:加入新制的氢氧化铜浊液,加热至沸腾,过滤取溶液
②除去福尔马林中少量的蚁酸:加入足量饱和碳酸钠溶液,充分振荡、蒸馏,收集馏出物
③除去苯中少量的苯酚:加溴水,振荡,过滤除去沉淀
④除去乙醇中少量的水:加足量新制生石灰,蒸馏.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
8.下列各组中属于同位素关系的是( )
| A. | ${\;}_{19}^{40}$K与${\;}_{20}^{40}$Ca | B. | T2O与 H2O | ||
| C. | ${\;}_{19}^{40}$K与${\;}_{19}^{39}$K | D. | 石墨和碳纳米管 |
18.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 碘和四氯化碳 | B. | 汽油和柴油 | C. | 水和四氯化碳 | D. | 水和醋酸 |
5.将下列物质按酸、碱、盐分类顺序排列正确的是( )
| A. | 硝酸 小苏打 硫酸钾 | B. | 硅酸 熟石灰 生石灰 | ||
| C. | 硫酸 烧碱 硫酸铝 | D. | 盐酸 纯碱 食盐 |
 一定温度下,在一容积不变的容器中,发生化学反应aA(g)+bB(g)═cC(g),采用不同比例的A,B作为起始物,测量反应达平衡时A和B的转化率,得到如图图象:
一定温度下,在一容积不变的容器中,发生化学反应aA(g)+bB(g)═cC(g),采用不同比例的A,B作为起始物,测量反应达平衡时A和B的转化率,得到如图图象: