题目内容
1.标准状况下的下列气体关系正确的是( )①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3.
| A. | 体积:④>①>②>③ | B. | 密度:②>③>①>④ | ||
| C. | 质量:②>③>①>④ | D. | 氢原子数:①>②>③>④ |
分析 结合n=$\frac{V}{Vm}$、n=$\frac{N}{{N}_{A}}$、n=$\frac{m}{M}$、$ρ=\frac{Mr}{Vm}$及分子构成计算.
解答 解:①6.72L CH4的物质的量为$\frac{6.72L}{22.4L/mol}$=0.3mol,②3.01×1023个HCl分子的物质的量为$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}}$=0.5mol,③13.6g H2S的物质的量为$\frac{13.6g}{34g/mol}$=0.4mol,④0.2mol NH3.
A.由V=nVm可知,物质的量越大,体积越大,则体积:②>③>①>④,故A错误;
B.由$ρ=\frac{Mr}{Vm}$可知,相对分子质量越大,密度越大,则密度为③>②>④>①,故B错误;
C.由m=nM可知,质量:②(0.5mol×36.5g/mol=18.25g)>③(13.6g)>①(0.3mol×16g/mol=4.8g)>④(0.2mol×17g/mol=3.4g),故C正确;
D.由分子构成可知,含氢原子的物质的量分别为1.2mol、0.5mol、0.8mol、0.6mol,则氢原子数:①>③>④>②,故D错误;
故选C.
点评 本题考查物质的量的计算,为高频考点,把握物质的量为中心的基本计算公式为解答的关键,侧重分析与计算能力的考查,注意密度的比较方法,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11. 向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示.沉淀的生成与溶解的pH列于下表.以下推断正确的是( )
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示.沉淀的生成与溶解的pH列于下表.以下推断正确的是( )
 向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示.沉淀的生成与溶解的pH列于下表.以下推断正确的是( )
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示.沉淀的生成与溶解的pH列于下表.以下推断正确的是( )| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | - | - |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| A. | AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-═2BaSO4↓+Al(OH)3↓ | |
| B. | C点的沉淀为Fe(OH)3 | |
| C. | OA段可能发生的反应是:3Ba2++6OH-+3SO42-+Fe3++Al3+═3BaSO4↓+Fe(OH)3↓+Al(OH)3↓ | |
| D. | 据图计算原溶液中c(Cl-)>c(SO42-) |
12.如图装置就用于实验室制取NH3,并用AlCl3溶液吸收多余氨气制氢氧化铝,最后回收氯化铵的实验,能达到实验目的是( )
| A. | 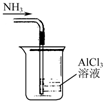 吸收NH3制取Al(OH)3 | |
| B. | 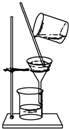 在不断搅拌下分离Al(OH)3和NH4Cl溶液 | |
| C. | 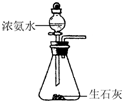 制取NH3 | |
| D. |  蒸干NH4Cl溶液并灼烧制NH4Cl |
16.1919年,科学家实现了人类多年的梦想--人工转变元素.这个核反应如下:$\stackrel{14}{7}$N+$\stackrel{4}{2}$He→${\;}_{8}^{17}$O+$\stackrel{1}{1}$H,下列有关叙述正确的是( )
| A. | ${\;}_{8}^{17}$O原子核内有9个质子 | |
| B. | $\stackrel{1}{1}$H原子核内有1个中子 | |
| C. | O2和O3互为同位素 | |
| D. | 通常情况下,He和N2化学性质都稳定 |
6.以下说法正确的是( )
| A. | 氢键属于化学键,但比较弱 | |
| B. | 任何物质中都一定含有化学键 | |
| C. | NaOH中有离子键和共价键,则NaOH既属于离子化合物,又属于共价化合物 | |
| D. | Na2O2中既有离子键,又有非极性共价键 |
13.下列关于聚丙烯酸酯(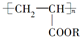 )的说法中,不正确的是( )
)的说法中,不正确的是( )
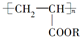 )的说法中,不正确的是( )
)的说法中,不正确的是( )| A. | 合成它的小分子化合物是CH3-CH2-COOR | |
| B. | 它可由CH2═CH-COOR经过加成聚合反应而得到 | |
| C. | 在一定条件下能发生水解反应 | |
| D. | 不能发生加成反应 |
10.下列离子方程式不正确的是( )
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| B. | 氨水中通入过量SO2:NH3•H2O+SO2═HSO3-+NH4+ | |
| C. | 饱和碳酸氢钙溶液中加入饱和氢氧化钙溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| D. | 氢氧化钙溶液与等物质的量的稀硫酸混合:Ca2++OH-+H++SO42-═CaSO4↓+H2O |