题目内容
按要求写出方程式.
(1)H++OH-=H2O(写出对应的化学方程式)
(2)氢氧化钡溶液和硫酸铜溶液(写出离子方程式)
(3)Fe2(SO4)3(写出电离方程式)
(4)将少量氢氧化钡溶液滴入碳酸氢钠溶液中(写出离子方程式) .
(1)H++OH-=H2O(写出对应的化学方程式)
(2)氢氧化钡溶液和硫酸铜溶液(写出离子方程式)
(3)Fe2(SO4)3(写出电离方程式)
(4)将少量氢氧化钡溶液滴入碳酸氢钠溶液中(写出离子方程式)
考点:离子方程式的书写
专题:离子反应专题
分析:(1)该离子方程式表示强酸与可溶性强碱溶液反应生成可溶性盐和水的反应;
(2)氢氧化钡与硫酸铜溶液反应生成硫酸钡沉淀和氢氧化铜沉淀;
(3)硫酸铁为强电解质,溶液中完全电离出铁离子和硫酸根离子;
(4)氢氧化钡少量,钡离子不足,反应生成碳酸钡沉淀和碳酸根离子.
(2)氢氧化钡与硫酸铜溶液反应生成硫酸钡沉淀和氢氧化铜沉淀;
(3)硫酸铁为强电解质,溶液中完全电离出铁离子和硫酸根离子;
(4)氢氧化钡少量,钡离子不足,反应生成碳酸钡沉淀和碳酸根离子.
解答:
解:(1)H++OH-=H2O表示可溶性强碱与强酸反应生成可溶性盐和水的反应,如:HCl+NaOH=NaCl+H2O,
故答案为:HCl+NaOH=NaCl+H2O;
(2)氢氧化钡与硫酸铜溶液反应生成氢氧化铜和硫酸钡沉淀,反应的离子方程式为:Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓
故答案为:Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓;
(3)硫酸铁在溶液中电离出铁离子和硫酸根离子,电离方程式为:Fe2(SO4)3=2Fe3++3SO42-,
故答案为:Fe2(SO4)3=2Fe3++3SO42-;
(4)氢氧化钡不足,反应生成碳酸钙沉淀和碳酸根离子,反应的离子方程式为:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O,
故答案为:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O.
故答案为:HCl+NaOH=NaCl+H2O;
(2)氢氧化钡与硫酸铜溶液反应生成氢氧化铜和硫酸钡沉淀,反应的离子方程式为:Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓
故答案为:Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓;
(3)硫酸铁在溶液中电离出铁离子和硫酸根离子,电离方程式为:Fe2(SO4)3=2Fe3++3SO42-,
故答案为:Fe2(SO4)3=2Fe3++3SO42-;
(4)氢氧化钡不足,反应生成碳酸钙沉淀和碳酸根离子,反应的离子方程式为:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O,
故答案为:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O.
点评:本题考查了离子方程式的书写,该题是高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,如难溶物、弱电解质等需要保留化学式.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
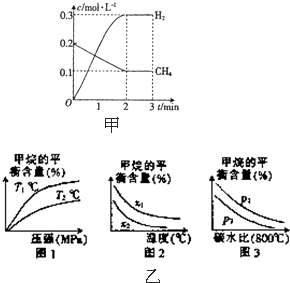 工业上利用天然气(主要成分是CH4)与H2O进行重整制备合成气(CO+H2),CO和H2在一定条件下能制备甲醛、甲醚和葡萄糖等多种有机物.
工业上利用天然气(主要成分是CH4)与H2O进行重整制备合成气(CO+H2),CO和H2在一定条件下能制备甲醛、甲醚和葡萄糖等多种有机物.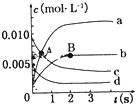 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表: