题目内容
9.四种短周期元素在周期表中的位置如图,其中只有M为金属元素,下列说法不正确的是( )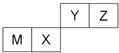
| A. | 原子半径Z<M | |
| B. | Z位于元素周期表中第2周期、第ⅥA族 | |
| C. | X的最简单气态氢化物的热稳定性比Z的小 | |
| D. | X的最高价氧化物不溶于任何酸 |
分析 由短周期元素在周期表中的位置可知,Y、Z处于第二周期,M、X处于第三周期,其中只有M为金属元素,可推知M为Al、X为Si、Y为N、Z为O.
A.同周期自左到右原子半径逐渐减小,同主族自上而下原子半径增大;
B.主族元素周期数=电子层数,族序数=最外层电子数;
C.元素非金属性越强,气态氢化物的稳定性越强;
D.二氧化硅可以溶液氢氟酸.
解答 解:由短周期元素在周期表中的位置可知,Y、Z处于第二周期,M、X处于第三周期,其中只有M为金属元素,可推知M为Al、X为Si、Y为N、Z为O.
A.同周期自左到右原子半径逐渐减小,同主族自上而下原子半径增大,因此原子半径O<Al,故A正确;
B.O原子含有2个电子层,最外层含有6个电子,因此O位于元素周期表中第二周期第ⅥA族,故B正确;
C.由于非金属性:O>Si,所以气态氢化物的稳定性:H2O>SiH4,故C正确;
D.二氧化硅可以溶液氢氟酸,故D错误,
故选:D.
点评 本题考查元素周期表与元素周期律的综合应用,比较基础,熟练掌握短周期元素,注意对元素周期律的理解掌握.

练习册系列答案
相关题目
19.下列叙述错误的是( )
| A. | 金属钠在自然界中可以以单质形式存在 | |
| B. | 金属钠燃烧时发出黄色火焰 | |
| C. | 金属钠保存在煤油中 | |
| D. | 金属钠在空气中燃烧生成过氧化钠 |
20. 已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )
已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )
 已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )
已知反应A(g)+B(g)?nC(g)△H=x kJ•mol-1,在不同条件下进行时,混合物中C的百分含量随时间变化的关系如右图.下列有关叙述一定正确的是( )| A. | a条件下的反应速率小于b条件下的反应速率 | |
| B. | 其他条件相同时,a表示有催化剂,b表示无催化剂 | |
| C. | 其他条件相同,若a、b表示不同压强下的反应,则n>2 | |
| D. | 其他条件相同,若a、b表示不同温度下的反应,则x>0 |
17.下列离子方程式正确的是( )
| A. | 澄清石灰水与稀盐酸反应:Ca(OH)2+2H+═Ca2++2H20 | |
| B. | 碳酸钠溶液与少量盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| C. | 稀硫酸与氢氧化钡溶液反应:H++OH-+Ba2++SO42-═H2O+BaSO4↓ | |
| D. | 氢氧化铜与稀硫酸反应:Cu(OH)2+2H+═Cu2++2H2O |
17.下列说法正确的是( )
| A. | 可以用澄清的石灰水鉴别SO2和CO2 | |
| B. | SO2能使溴水、KMnO4溶液迅速褪色 | |
| C. | 硫粉在过量的氧气中燃烧可得到SO3 | |
| D. | 少量SO2通入到浓的CaCl2溶液能生成白色沉淀 |
18.下列有关化学用语正确的是( )
| A. | 乙醇、乙二醇、丙三醇互为同系物,同系物之间不可能为同分异物体 | |
| B. | 北京奥运会奖牌--“金镶玉”奖牌玉的化学成分多为含水钙镁硅酸盐,如:Ca2Mg5Si8O22(OH)2可用氧化物表示为:2CaO•5MgO•8SiO2•H2O | |
| C. | 次氯酸的结构式为:H-Cl-O | |
| D. | 丙烷分子的比例模型示意图: |