题目内容
4.用过量锌与稀硫酸反应制H2时,下列能延缓反应速率但又不影响生成氢气总量的是( )| A. | 加入少量NaNO3溶液 | B. | 加入少量CuSO4溶液 | ||
| C. | 加入少量蒸馏水 | D. | 改用98%的浓硫酸 |
分析 过量的锌粉反应,稀硫酸完全反应,为了减缓反应速率但又不影响生成氢气的总量,可减小氢离子浓度但不改变其物质的量;注意稀硝酸、浓硫酸与锌反应生成的不是氢气,据此进行解答.
解答 解:A.加入硝酸钠溶液后,硝酸根离子在酸性条件下具有强氧化性,与锌反应生成NO,影响了氢气的量,故A错误;
B.加入硫酸铜溶液,锌与铜离子反应生成铜,锌与铜形成原电池,加快了反应速率,故B错误;
C.加入少量蒸馏水,稀硫酸被稀释,反应速率减小,且生成氢气的总量不变,故C正确;
D.改用98%的浓硫酸,锌与浓硫酸反应生成的是二氧化硫,不会生成氢气,故D错误;
故选C.
点评 本题考查了影响化学反应速率的因素,题目难度不大,明确题干暗含条件的含义为解答关键,注意掌握化学反应速率及其影响因素,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
15.下列有关化学用语表示正确的是( )
| A. | 质量数为35的氯原子:${\;}_{35}^{17}$Cl | |
| B. | 14C的原子结构示意图: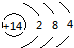 | |
| C. | N2分子的电子式: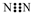 | |
| D. | 乙酸乙酯的结构简式为:CH3COOC2H5 |
12.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑨九种元素在周期表中的位置.
请回答:
(1)以上元素中,最高价氧化物对应水化物酸性最强的是HClO4;碱性最强的是KOH;显两性的是Al(OH)3(填化学式)
(2)③、④、⑨三种元素按原子半径由大到小的顺序依次为K>Na>Mg(填元素符号)
(3)按要求写出下列两种物质的电子式:⑥的氢化物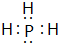 ; ⑨的最高价氧化物的对应的水化物
; ⑨的最高价氧化物的对应的水化物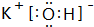 ;
;
(4)由H和①形成的原子数之比为1:1的物质H2O2 (填化学式).
(5)利用⑧的单质制备漂白粉发生反应的化学方程式为2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
(6)⑤的最高价氧化物对应的水化物既能与③的最高价氧化物对应的水化物反应,也能与⑧的最高价氧化物对应的水化物反应.分别写出其反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;Al(OH)3+3H+=Al3++3H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ |
(1)以上元素中,最高价氧化物对应水化物酸性最强的是HClO4;碱性最强的是KOH;显两性的是Al(OH)3(填化学式)
(2)③、④、⑨三种元素按原子半径由大到小的顺序依次为K>Na>Mg(填元素符号)
(3)按要求写出下列两种物质的电子式:⑥的氢化物
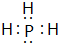 ; ⑨的最高价氧化物的对应的水化物
; ⑨的最高价氧化物的对应的水化物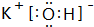 ;
;(4)由H和①形成的原子数之比为1:1的物质H2O2 (填化学式).
(5)利用⑧的单质制备漂白粉发生反应的化学方程式为2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2H2O.
(6)⑤的最高价氧化物对应的水化物既能与③的最高价氧化物对应的水化物反应,也能与⑧的最高价氧化物对应的水化物反应.分别写出其反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O;Al(OH)3+3H+=Al3++3H2O.
19.用价层电子对互斥理论预测H2S和PCl3的立体结构,两个结论都正确的是( )
| A. | 直线形;三角锥形 | B. | V形;三角锥形 | ||
| C. | 直线形;平面三角形 | D. | V形;平面三角形 |
16.有关化学键的说法正确的是( )
| A. | 全部由非金属元素构成的化合物一定是共价化合物 | |
| B. | 某元素的原子最外层只有一个电子,它跟卤素结合时,所形成的化学键一定是离子键 | |
| C. | 金属与非金属原子间只能形成离子键 | |
| D. | 含有共价键的化合物不一定是共价化合物 |
13.维生素C的结构简式为 ,丁香油酚的结构简式为:
,丁香油酚的结构简式为: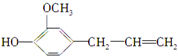 ,下列关于两者的说法正确的是( )
,下列关于两者的说法正确的是( )
 ,丁香油酚的结构简式为:
,丁香油酚的结构简式为: ,下列关于两者的说法正确的是( )
,下列关于两者的说法正确的是( )| A. | 均含酯基 | B. | 均含碳碳双键 | ||
| C. | 均含醇羟基和酚羟基 | D. | 均为芳香化合物 |
14.下列物质①乙烷②乙炔③甲苯④苯乙烯⑤聚乙烯⑥苯酚⑦乙醇,其中既能与溴水反应又能与酸性高锰酸钾溶液反应的是( )
| A. | ②③④⑤ | B. | ②④⑥ | C. | ②③④⑤⑥⑦ | D. | ②⑤⑥ |

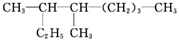 3,4-二甲基辛烷
3,4-二甲基辛烷 ,1mol该烃完全燃烧需消耗氧气18.5mol.
,1mol该烃完全燃烧需消耗氧气18.5mol.