题目内容
在恒容的密闭容器中,可逆反应X(s)+3Y(g)?2Z(g);△H>0,达到平衡时,下列说法正确的是( )
| A、充入少量He使容器内压强增大,平衡向正反应方向移动 |
| B、升高温度,平衡向正反应方向移动,平均分子量变小 |
| C、继续加入少量X,X的转化率减小,Y的转化率增大 |
| D、继续加入少量Y,再次平衡时,Y的体积分数比上次平衡小 |
考点:化学平衡的影响因素
专题:原子组成与结构专题
分析:A、恒容容器中加入惰气,总压增大,分压不变,平衡不移动;
B、反应是吸热反应升温平衡正向进行,气体物质的量减小,总质量变大,所以平均分子量变大;
C、X为固体,改变用量不影响化学平衡;
D、继续加入少量Y,根据先放大在压缩,平衡向正反应方向移动来判断.
B、反应是吸热反应升温平衡正向进行,气体物质的量减小,总质量变大,所以平均分子量变大;
C、X为固体,改变用量不影响化学平衡;
D、继续加入少量Y,根据先放大在压缩,平衡向正反应方向移动来判断.
解答:
解:A、恒容容器中加入惰气,总压增大,分压不变,平衡不移动,故A错误;
B、反应是吸热反应升温平衡正向进行,气体物质的量减小,总质量变大,所以平均分子量变大,故B错误;
C、X为固体,改变用量不影响化学平衡,增加X的用量,化学平衡不发生移动,故C错误;
D、继续加入少量Y,根据先放大在压缩,平衡向正反应方向移动,所以再次平衡时,Y的体积分数比上次平衡小,故D正确;
故选D.
B、反应是吸热反应升温平衡正向进行,气体物质的量减小,总质量变大,所以平均分子量变大,故B错误;
C、X为固体,改变用量不影响化学平衡,增加X的用量,化学平衡不发生移动,故C错误;
D、继续加入少量Y,根据先放大在压缩,平衡向正反应方向移动,所以再次平衡时,Y的体积分数比上次平衡小,故D正确;
故选D.
点评:本题考查了化学平衡影响因素分析,平衡移动原理的分析判断是解题关键,题目较简单.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
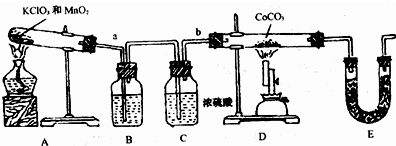
下列实验装置图完全正确的是( )
A、 |
B、 |
C、 |
D、 |
禁止使用含磷洗衣粉(三聚磷酸钠Na5P3O10)原因是( )
| A、会刺激皮肤 |
| B、会腐蚀下水道 |
| C、会引起白色污染 |
| D、会造成水质富营养化,使水质变坏 |
若溶液中由水电离产生的c(OH-)=1×10-14mol?L-1,满足条件的溶液中一定可以大量共存的离子组是( )
| A、Al3+,Na+,NO3-,Cl- |
| B、K+,Na+,Cl-,NO3- |
| C、K+,Na+,Cl-,CH3COO- |
| D、K+,NH4+,SO42-,NO3- |
下列离子方程式正确的是( )
| A、三氯化铝溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ |
| B、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ |
| C、K37ClO3与浓盐酸(HCl)在加热时生成氯气:K37ClO3+6HCl=K37Cl+3Cl2↑+3H2O |
| D、将0.1mol/L盐酸数滴缓缓滴入0.1mol/L25mLNa2CO3溶液中,并不断搅拌:2H++CO32-═CO2↑+H2O |
等质量的三份铁a、b和c,分别加入到足量稀H2SO4中,a中同时加入适量CuSO4溶液,c中同时加入适量CH3COOK.下列各图中表示其产生氢气总体积(V)与时间(t)的关系,其中正确的是( )
A、 |
B、 |
C、 |
D、 |
下列有关中和热和燃烧热的说法中,正确的是( )
| A、进行中和热测定的实验时,不能用环形铁质搅拌棒代替环形玻璃搅拌棒 |
| B、用等体积的0.50mol?L-1盐酸和0.55mol?L-1NaOH溶液进行中和热测定的实验,会使测定结果偏大 |
| C、已知强酸与强碱反应的中和热△H=-57.3kJ?mol-1.所以,1L 1mol?L-1H2SO4与稀NaOH溶液恰好完全反应时,放出57.3kJ的热量 |
| D、已知2C(s)+O2(g)=2CO(g)△H=-220.7kJ?mol-1;所以,C的燃烧热是△H=-220.7kJ?mol-1 |
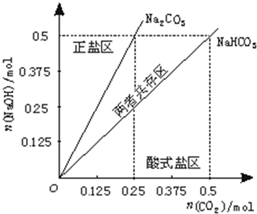 用NaOH、H2O、大理石和盐酸制取33g纯NaHCO3,请参照物质的溶解度回答下列问题:
用NaOH、H2O、大理石和盐酸制取33g纯NaHCO3,请参照物质的溶解度回答下列问题: