题目内容
15.能用H++OH-═H2O来表示的化学反应是( )| A. | 纯碱与盐酸反应 | B. | Ba(OH)2和H2SO4溶液反应 | ||
| C. | KOH溶液和亚硫酸溶液反应 | D. | NH4HSO4溶液和少量NaOH溶液反应 |
分析 离子方程式H++OH-═H2O表示可溶性强碱与强酸反应生成可溶性盐和水的一类反应,据此进行解答.
解答 解:A.碳酸钠与盐酸的反应为:2H++CO32-═CO2↑+H2O,不能用H++OH-═H2O来表示,故A错误;
B.Ba(OH)2和H2SO4溶液反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,不能用H++OH-═H2O来表示,故B错误;
C.KOH溶液和亚硫酸溶液反应的离子方程式为:OH-+HCO3-═CO32-+H2O,不能用H++OH-═H2O来表示,故C错误;
D.NH4HSO4溶液和少量NaOH溶液反应时生成硫酸钠、硫酸铵和水,反应的离子方程式为:H++OH-═H2O,故D正确;
故选D.
点评 本题考查了离子方程式的判断,题目难度不大,注意掌握离子方程式的书写原则,明确离子方程式表示的意义为解答关键,试题培养了学生的分析能力及规范答题能力.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
5.下列原子轨道重叠时,能形成π键的是( )
| A. | 只有py与py | B. | 只有pz与pz | ||
| C. | 只有dxy与py | D. | 上述三种情况都能 |
6.下列物质中熔点高低关系正确的是( )
| A. | NaCl>NaF | B. | BaO>CaO | C. | H2S>H2O | D. | SiO2>CO2 |
3.1mol•L-1 NaCl溶液的含义是( )
| A. | 1L水中含有1mol NaCl | |
| B. | 溶液中含有1mol NaCl | |
| C. | 1L溶液中含有58.5g NaCl | |
| D. | 将58.5g NaCl溶于1L水中所得的溶液 |
10.下列有关仪器使用方法或实验操作正确的是( )
| A. | 可以用酒精灯直接加热锥形瓶和容量瓶 | |
| B. | 用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体 | |
| C. | 蒸馏时温度计水银球应高于蒸馏烧瓶支管口 | |
| D. | 振荡分液漏斗时应关闭其玻璃塞和活塞 |
 “大象牙膏”的实验操作是向30%的过氧化氢溶液中加入少量二氧化锰和表面活性剂,现象如图.
“大象牙膏”的实验操作是向30%的过氧化氢溶液中加入少量二氧化锰和表面活性剂,现象如图.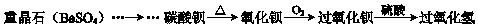
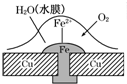 金属腐蚀是我们日常生活的常见现象.请根据如图回答下列问题:
金属腐蚀是我们日常生活的常见现象.请根据如图回答下列问题: