题目内容
20.氯是常见的非金属单质.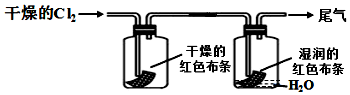
(1)氯气与铁反应的化学方程式为2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(2)新制的氯水呈黄绿色,说明氯水中存在Cl2(写化学式),向氯水中滴入几滴AgNO3溶液,现象是生成白色沉淀,离子方程式为Ag++Cl-=AgCl↓.
(3)将干燥的氯气依次通过盛有干燥红色布条和湿润红色布条的广口瓶(如图所示),现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.为防止氯气污染,可用NaOH溶液吸收尾气,该反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O.
分析 (1)氯气与铁反应生成氯化铁;
(2)新制氯水中存在Cl2+H2O?HCl+HClO,所以新制氯水中存在Cl2、HClO、H2O、H+、Cl-、ClO-、OH-,其中HClO具有漂白性和强氧化性,结合对应物质的性质解答;
(3)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性;氯气可与氢氧化钠反应,可用于吸收氯气.
解答 解:(1)氯气与铁反应生成氯化铁,反应的方程式为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故答案为:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
(2)新制氯水中存在Cl2+H2O?HCl+HClO,因含有氯气,则溶液呈淡黄绿色,向氯水中滴入几滴AgNO3溶液,发生离子反应方程式为:Ag++Cl-=AgCl↓,生成白色沉淀,说明溶液中含有Cl-,故答案为:Cl2;生成白色沉淀;Ag++Cl-=AgCl↓;
(3)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性,干燥的有色布条无明显现象,潮湿的有色布条褪色;氯气可与氢氧化钠反应,可用于吸收氯气,反应的方程式为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:干燥的有色布条无明显现象,潮湿的有色布条褪色;NaOH; Cl2+2NaOH=NaCl+NaClO+H2O.
点评 本题综合考查元素化合物知识,侧重于氯气性质的考查,为高频考点,注意相关基础知识的积累,难度不大.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
11.下列事实能说明物质的性质影响化学反应速率的是( )
| A. | 常温下,二氧化锰与浓盐酸不反应,而高锰酸钾与浓盐酸反应产生氯气 | |
| B. | 接触面相近的锌粒与1mo1•L-1的盐酸反应比1mo1•L-1的硫酸反应快 | |
| C. | 同质量的煤块在空气中燃烧比煤粉燃烧要慢 | |
| D. | 甲烷与氯气的混合气体在暗室中黄绿色变浅速率比在太阳照射下慢 |
8.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1LpH=1的溶液中含有的H+数目为NA | |
| B. | 常温常压下,22.4LCH4含有的分子数为NA | |
| C. | 1molNa2O2固体中含有的离子总数为3NA | |
| D. | 1mol•L-1NaCl溶液中含有的Cl-数目为NA |
15.能用H++OH-═H2O来表示的化学反应是( )
| A. | 纯碱与盐酸反应 | B. | Ba(OH)2和H2SO4溶液反应 | ||
| C. | KOH溶液和亚硫酸溶液反应 | D. | NH4HSO4溶液和少量NaOH溶液反应 |
5.东晋炼丹家葛洪的《抱朴子》里记载“丹砂(HgS)烧之成水银,积变又还成丹砂”这句话里没有涉及到的反应类型为( )
| A. | 置换反应 | B. | 化合反应 | C. | 分解反应 | D. | 氧化还原反应 |
12.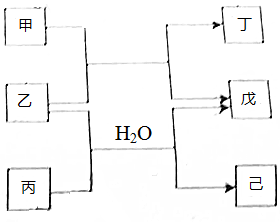 短周期元素E,R,X,Y,Z的原子序数依次增大,它们组成的单质或化合物存在如图转化关系,甲、丁为二元化合物,乙戊为单质,丙和已为三元化合物.25℃时,0.1 mol•L-1甲溶液的pH=1,0.1mol•L-1丙溶液的pH=13.丁、己溶液混合时产生白色沉淀,下列推断不正确的是( )
短周期元素E,R,X,Y,Z的原子序数依次增大,它们组成的单质或化合物存在如图转化关系,甲、丁为二元化合物,乙戊为单质,丙和已为三元化合物.25℃时,0.1 mol•L-1甲溶液的pH=1,0.1mol•L-1丙溶液的pH=13.丁、己溶液混合时产生白色沉淀,下列推断不正确的是( )
 短周期元素E,R,X,Y,Z的原子序数依次增大,它们组成的单质或化合物存在如图转化关系,甲、丁为二元化合物,乙戊为单质,丙和已为三元化合物.25℃时,0.1 mol•L-1甲溶液的pH=1,0.1mol•L-1丙溶液的pH=13.丁、己溶液混合时产生白色沉淀,下列推断不正确的是( )
短周期元素E,R,X,Y,Z的原子序数依次增大,它们组成的单质或化合物存在如图转化关系,甲、丁为二元化合物,乙戊为单质,丙和已为三元化合物.25℃时,0.1 mol•L-1甲溶液的pH=1,0.1mol•L-1丙溶液的pH=13.丁、己溶液混合时产生白色沉淀,下列推断不正确的是( )| A. | 简单离子半径:r(Z)>r(R)>r(X)>r(Y) | |
| B. | X,Y,Z的最高价氧化物对应的水化物相互反应 | |
| C. | R,E,Z可存在于同一种共价化合物中 | |
| D. | Z的阴离子夺质子能力较R的阴离子强 |
17.下列物质属于电解质的是( )
| A. | 金属铜 | B. | 氯化钠溶液 | C. | 硝酸钾固体 | D. | 二氧化碳 |
18.欲配制pH=13.00的溶液10.0dm3,所需NaOH固体的质量是(相对原子质量:Na 23)( )
| A. | 40g | B. | 4.0g | C. | 4.0×10-11g | D. | 4.0×10-12g |