题目内容
11.常温下,NC13是一种油状液体,其分子空间构型为三角锥形,下列对NC13的有关叙述错误的是( )| A. | NC13中N-C1键键长比CCl4中C-C1键键长短 | |
| B. | NC13分子中的所有原子均达到8电子稳定结构 | |
| C. | NCl3分子是极性分子 | |
| D. | NBr3的沸点比NCl3的沸点低 |
分析 A.原子半径越小,原子间形成的键长越短;
B.如果元素的最外层电子数+元素的化合价的绝对值=8,该元素就达到8电子稳定结构,否则没有达到8电子稳定结构;
C.根据该分子是否是对称结构判断分子的极性;
D.无氢键的分子晶体相对分子质量越大其熔沸点越高;
解答 解:A.C原子的原子半径大于N原子的原子半径,所以CCl4中C-C1键键长比NC13中N-C1键键长,故A正确;
B.NC13中N原子最外层电子数5+化合价的绝对值3=8,所以N原子达到8电子稳定结构;NC13中C1原子最外层电子数7+化合价的绝对值1=8,所以C1原子达到8电子稳定结构,故B正确;
C.NC13的分子空间构型是三角锥型结构不是正四面体结构,NCl3分子空间构型不对称,所以NCl3分子是极性分子,故C正确;
D.无氢键的分子晶体中物质的熔沸点与相对分子质量有关,相对分子质量越大其熔沸点越高,所以NBr3比NCl3的熔沸点高,故D错误;
故选D.
点评 本题考查NC13的有关知识,明确微粒半径大小比较、化合物中原子最外层电子数是否为8的判断方法、熔沸点大小的判断方法是解答关键,题目难度中等.

练习册系列答案
相关题目
19.为了避免NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理(反应方程式:2NO2+2NaOH=NaNO2+H2O;NO2+NO+2NaOH=2NaNO2+H2O).现有由a mol NO、b molNO2、c molN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度为( )
| A. | $\frac{a+b+c}{V}$molgL-1 | B. | $\frac{a+b+2c}{V}$molgL-1 | C. | $\frac{2a+b+c}{V}$molgL-1 | D. | $\frac{b+2c}{V}$molgL-1 |
1.硫酸钠是一种重要的化工原料,其溶解度曲线如图所示.下列说法正确的是( )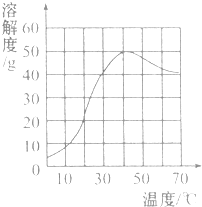

| A. | 硫酸钠的溶解度随温度升高而增大 | |
| B. | 30℃时硫酸钠饱和溶液的质量分数为40% | |
| C. | 40℃时硫酸钠的溶解度约为50g | |
| D. | 60℃时硫酸钠饱和溶液降温后一定饱和 |
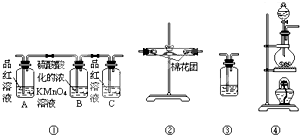 已知:SO2可以与硫酸酸化的浓KMnO4溶液反应,也可以使澄清的石灰水变浑浊.如图④中浓硫酸与木炭粉在加热条件下发生反应生成CO2、SO2和H2O.
已知:SO2可以与硫酸酸化的浓KMnO4溶液反应,也可以使澄清的石灰水变浑浊.如图④中浓硫酸与木炭粉在加热条件下发生反应生成CO2、SO2和H2O.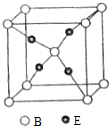
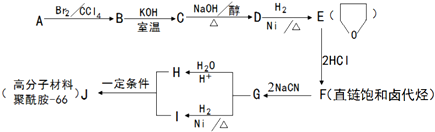
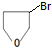 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$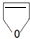 +NaBr+H2O.
+NaBr+H2O.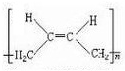 .
.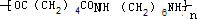 +2nH2O.
+2nH2O.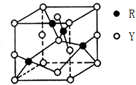 X、Y、Z、R为前四周期元素,原子序数依次增大.X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素;R+离子的3d轨道全充满.
X、Y、Z、R为前四周期元素,原子序数依次增大.X、Y同周期,X基态原子的最外层电子数是次外层的2倍,Y基态原子的s能级和p能级上电子数相等;Z是地壳中含量最高的金属元素;R+离子的3d轨道全充满.