题目内容
 化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示.下列说法不正确的是( )
化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示.下列说法不正确的是( )| A、A为电源正极 |
| B、阳极反应式为:2H2O-4e-═4H++O2↑ |
| C、若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为10.4克 |
| D、阴极反应式为:2NO3-+6H2O+10e-=N2↑+12OH- |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.该装置中,硝酸根离子得电子发生还原反应,则Ag-Pt电极为阴极、Pt电极为阳极,连接阳极的电极为正极;
B.阳极上水失电子发生氧化反应;
C.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室;
D.阴极上硝酸根离子得电子发生还原反应.
B.阳极上水失电子发生氧化反应;
C.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室;
D.阴极上硝酸根离子得电子发生还原反应.
解答:
解:A.根据图知,电解槽右边部分N元素化合价由+5价变为0价,所以硝酸根离子发生还原反应,则Ag-Pt电极为阴极、Pt电极为阳极,所以A是正极、B是负极,故A正确;
B.阳极上水失电子生成氢离子和氧气而发生氧化反应,电极反应式为2H2O-4e-═4H++O2↑,故B正确;
C.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极的电极反应式为2NO3-+6H++10e-=N2↑+6OH-,转移2mol电子,阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室,因此阴极室质量减少3.6g,故膜两侧电解液的质量变化差(△m左-△m右)=18g-3.6g=14.4g,故C错误;
D.阴极上硝酸根离子得电子发生还原反应,电极反应式为2NO3-+6H2O+10e-=N2↑+12OH-,故D正确;
故选C.
B.阳极上水失电子生成氢离子和氧气而发生氧化反应,电极反应式为2H2O-4e-═4H++O2↑,故B正确;
C.转移2mol电子时,阳极(阳极反应为H2O失电子氧化为O2和H+)消耗1mol水,产生2molH+进入阴极室,阳极室质量减少18g;阴极的电极反应式为2NO3-+6H++10e-=N2↑+6OH-,转移2mol电子,阴极室中放出0.2molN2(5.6g),同时有2molH+(2g)进入阴极室,因此阴极室质量减少3.6g,故膜两侧电解液的质量变化差(△m左-△m右)=18g-3.6g=14.4g,故C错误;
D.阴极上硝酸根离子得电子发生还原反应,电极反应式为2NO3-+6H2O+10e-=N2↑+12OH-,故D正确;
故选C.
点评:本题考查了电解原理,根据N元素化合价变化确定阴阳极、正负极,难点是电极反应式的书写,易错选项是C,注意氢离子还进入阴极室,很多同学往往只考虑析出的气体而导致错误,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子在溶液中能大量共存的是( )
| A、SO42-、HCO3-、Na+、H+ |
| B、K+、SO42-、Fe3+、NO3- |
| C、H+、Na+、Cl-、CO32- |
| D、Ca2+、OH-、CO32-、Na+ |
液氨与水性质相似,也存在微弱的电离:2NH3→NH4++NH2-,某温度下其离子积常数K=c(NH4+)?c(NH2-)=2×l0-30,维持温度不变,向液氨中加入少量NH4Cl固体或NaNH2固体,不发生改变的是( )
| A、液氨的电离度 |
| B、液氨的离子积常数 |
| C、c(NH4+) |
| D、c(NH2-) |
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、0.1mol/L的氢氧化钠溶液中含钠离子数目为0.1NA |
| B、常温常压下,11.2L氮气所含的原子数目为NA |
| C、常温常压下,3.4g NH3所含的原子数目为0.8NA |
| D、78g Na2O2与足量水反应转移的电子数目为2NA |
将镁和铝两金属块用导线连接后插入盛有氢氧化钠溶液的烧杯中,发现镁片上有气泡产生,下列叙述正确的是( )
| A、上述装置构成原电池,镁的金属性比铝强是负极 |
| B、上述装置构成原电池,铝是负极是因为铝的金属性比镁强 |
| C、上述装置不构成原电池,铝只与氢氧化钠溶液直接发生置换反应 |
| D、负极的电极反应式为:Al+4OH--3e-=AlO2-+2H2O |
 如图为以惰性电极进行电解:
如图为以惰性电极进行电解: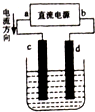 如图是电解CuCl2溶液的装置,其中c、d为石墨电极.
如图是电解CuCl2溶液的装置,其中c、d为石墨电极.