题目内容
将镁和铝两金属块用导线连接后插入盛有氢氧化钠溶液的烧杯中,发现镁片上有气泡产生,下列叙述正确的是( )
| A、上述装置构成原电池,镁的金属性比铝强是负极 |
| B、上述装置构成原电池,铝是负极是因为铝的金属性比镁强 |
| C、上述装置不构成原电池,铝只与氢氧化钠溶液直接发生置换反应 |
| D、负极的电极反应式为:Al+4OH--3e-=AlO2-+2H2O |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:将镁和铝两金属块用导线连接后插入盛有氢氧化钠溶液的烧杯中由于铝和氢氧化钠溶液反应,而镁与氢氧化钠溶液不反应,则铝为负极,镁为正极,负极反应为2Al+8OH--6e-=2AlO2-+4H2O,正极反应为6H2O+6e-=6OH-+3H2↑,以此解答.
解答:
解:镁比铝活泼,但由于镁和氢氧化钠溶液不反应,而铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,则铝为负极,镁为正极,负极反应为2Al+8OH--6e-=2AlO2-+4H2O,正极反应为6H2O+6e-=6OH-+3H2↑,
故选D.
故选D.
点评:本题考查原电池及常见的电池,明确电池的工作原理以及原电池的组成是解答该题的关键,注重基础知识的考查,题目难度不大,注意铝与氢氧化钠溶液反应的特点.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案
相关题目
分别用pH=2和pH=3的醋酸溶液中和等物质的量的苛性钾溶液,消耗两种醋酸溶液的体积分别为V1和V2,V1和V2的关系正确的是( )
| A、V2=10V1 |
| B、V1>10V2 |
| C、V2<10V1 |
| D、V2>10V1 |
化学反应的特征是( )
| A、发光 | B、能量发生变化 |
| C、状态发生变化 | D、发热 |
现有等体积的Ba(OH)2、NaOH和NH3?H2O三种溶液,将它们分别与V1 L、V2 L、V3 L等浓度的盐酸混合,下列说法中正确的是( )
| A、若混合前三溶液物质的量浓度相等,混合后溶液呈中性,则V1>V2=V3 |
| B、若混合前三溶液pH相等,酸碱恰好完全反应,则V1=V2<V3 |
| C、若混合前三溶液物质的量浓度相等,酸碱恰好完全反应,则V1=V2=V3 |
| D、若混合前三溶液pH相等,将它们同等倍数稀释后,则NaOH溶液pH最大 |
下列说法不正确的是( )

A、在25℃时,将c mol?L-1的醋酸溶液与0.02mol?L-1 NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=
| ||
| B、0.1mol?L-1醋酸溶液中:c(H+)2=c(H+)?c(CH3COO-)+KW | ||
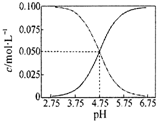
| C、常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如右图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | ||
| D、等体积等物质的量浓度的CH3COONa(aq)与NaCl(aq)中离子总数大小:N前>N后 |
 化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示.下列说法不正确的是( )
化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染.电化学降解NO3-的原理如图所示.下列说法不正确的是( )| A、A为电源正极 |
| B、阳极反应式为:2H2O-4e-═4H++O2↑ |
| C、若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为10.4克 |
| D、阴极反应式为:2NO3-+6H2O+10e-=N2↑+12OH- |