题目内容
17.目前我们生活中的食盐中往往要加“碘”,该成分主要是( )| A. | KI | B. | I2 | C. | I- | D. | KIO3 |
分析 加碘食盐中添加的是KIO3,据此解题.
解答 解:目前加碘食盐中主要添加的是KIO3.
故选D.
点评 本题考查碘与人体健康,侧重于常识性内容的考查,难度不大,注意基础知识的积累.

练习册系列答案
相关题目
5.关节炎病原因是在关节滑液中形成尿酸钠晶体:
HUr(尿酸)+H2O?Ur-(尿酸根离子)+H3O+
Ur-(溶液)+Na+(溶液)?NaUr(固)
第一次关节炎发作大部分在寒冷季节脚趾和手指的关节处.下列叙述不正确的是( )
HUr(尿酸)+H2O?Ur-(尿酸根离子)+H3O+
Ur-(溶液)+Na+(溶液)?NaUr(固)
第一次关节炎发作大部分在寒冷季节脚趾和手指的关节处.下列叙述不正确的是( )
| A. | 尿酸酸性比盐酸弱 | B. | 尿酸钠的溶解度随温度升高而增大 | ||
| C. | 反应①为吸热反应,②为放热反应 | D. | 尿酸钠的熔点很低 |
12.下列热化学方程式的书写正确的是( )
| A. | 1mol液态肼在足量氧气中完全燃烧生成水蒸气,放出642kJ的热量:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=+642 kJ•mol-1 | |
| B. | 101 kPa下,26 g乙炔在足量氧气中完全燃烧生成液态水,放出1 299.6 kJ的热量:C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(l)△H=-1 299.6 kJ | |
| C. | 12 g石墨转化为CO时,放出110.5 kJ的热量:2C(石墨,s)+O2(g)═2CO(g)△H=-110.5 kJ•mol-1 | |
| D. | 1 mol B2H6气体完全燃烧生成固态三氧化二硼和液态水,放出2 165 kJ的热量:B2H6(g)+3O2(g)═B2O3(s)+3H2O(l)△H=-2 165 kJ•mol-1 |
9.化学与生产、生活、社会密切相关.下列说法中不正确的是( )
| A. | 雪白、漂亮的“白木耳”,可能是在用硫黄熏制的过程中产生的SO2所致 | |
| B. | 钢铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| C. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| D. | 硅胶可用作食品干燥剂和催化剂载体 |
7.化学反应原理在工业生产中具有十分重要的意义.
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol.
(2)已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ•mol-1.测得在不同温度下,该反应的平衡常数K随温度的变化如下:
①该反应的化学平衡常数K的表达式为$\frac{c(CO)}{c(C{O}_{2})}$,a>0(填“>”、“<”或“=”).在500℃2L密闭容器中进行反应,Fe和CO2的起始量均为4mol,则5min后达到平衡时CO2的转化率为50%,生成CO的平均速率v(CO)为0.2mol/(Lmin).
②700℃反应达到平衡后,要使反应速率增大且平衡向右移动,可采取的措施有增加CO2的量或者升高温度.
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式CH3OH-6e-+H2O=CO2+6H+,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH=1(溶液电解前后体积的变化忽略不计).
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol.
(2)已知反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H=a kJ•mol-1.测得在不同温度下,该反应的平衡常数K随温度的变化如下:
| 温度(℃) | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
②700℃反应达到平衡后,要使反应速率增大且平衡向右移动,可采取的措施有增加CO2的量或者升高温度.
(3)利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式CH3OH-6e-+H2O=CO2+6H+,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2(标准状况下)时,电解后溶液的pH=1(溶液电解前后体积的变化忽略不计).
 二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应: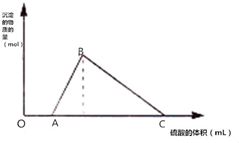 将M克钠和铝的混合物投入到一定量的水中,金属全部溶解,并收集到标准状况下体积为N升的气体,在所得溶液中逐滴加入1mol/L H2SO4,所得沉淀的物质的量随滴入硫酸溶液的体积变化如图所示;已知:A、C点对应的横坐标数据分别是500mL和2500mL,则
将M克钠和铝的混合物投入到一定量的水中,金属全部溶解,并收集到标准状况下体积为N升的气体,在所得溶液中逐滴加入1mol/L H2SO4,所得沉淀的物质的量随滴入硫酸溶液的体积变化如图所示;已知:A、C点对应的横坐标数据分别是500mL和2500mL,则