题目内容
13.氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过反应 Al2O3+N2+3C═2AlN+3CO合成,下列叙述正确是( )| A. | 反应中,N2是还原剂,Al2O3是氧化剂 | |
| B. | 反应中,每生成2 mol AlN,N2得到3 mol电子 | |
| C. | 氮化铝中氮元素的化合价为-3 | |
| D. | AlN的摩尔质量为41g |
分析 Al2O3+N2+3C═2AlN+3CO中,N元素的化合价降低,C元素的化合价升高,以此来解答.
解答 解:A.N元素的化合价降低,C元素的化合价升高,则C是还原剂,N2是氧化剂,故A错误;
B.反应中,每生成2 mol AlN,N2得到1mol×2×[0-(-3)]=6 mol电子,故B错误;
C.氮化铝中Al为+3价,则氮元素的化合价为0-3=-3价,故C正确;
D.AlN的摩尔质量为41g/mol,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答本题关键,侧重分析与应用能力的考查,注意转移电子的计算及元素的化合价判断,题目难度不大.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案
相关题目
3.下列说法中正确的是( )
| A. | 0.1 mol•L-1盐酸和0.1 mol•L-1硫酸与2 mol•L-1 NaOH溶液反应速率相同 | |
| B. | 大理石块和大理石粉与0.1 mol•L-1盐酸反应的速率相同 | |
| C. | 等量的Mg粉、Al粉和0.1 mol•L-1盐酸反应速率相同 | |
| D. | 0.1 mol•L-1盐酸和0.1 mol•L-1硝酸与相同形状和大小的大理石反应的速率相同 |
4.某有机化合物的结构简式如图所示,关于该化合物的下列说法正确的是( )


| A. | 由于含有氧元素不是有机物 | |
| B. | 完全燃烧时只有二氧化碳和水两种产物 | |
| C. | 属于醇 | |
| D. | 不能使溴水褪色 |
1.下面的烷烃是烯烃R和氢气发生加成反应后的产物,则R可能的结构简式有( )
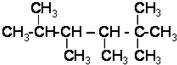

| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
8.下列说法正确的是( )
| A. | 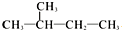 与 与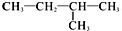 互为同分异构体 互为同分异构体 | |
| B. | CH3-CH2-CH3、CH3-CH2-CH2-CH2-CH3、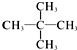 互为同系物,熔沸点逐渐升高 互为同系物,熔沸点逐渐升高 | |
| C. | 烷烃燃烧通式为:CnH2n+2+$\frac{3n+1}{2}$O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O | |
| D. | 分子式为C4H10O并能与金属钠反应放出氢气的有机物有3种 |
11.下列所述有机物中同分异构体种数最少的是(不考虑立体异构)( )
| 分子式 | 满足条件 | |
| A | C3H8O | 能与金属钠反应 |
| B | C5H8O4 | 有2个-COOH |
| C | C3H6O2 | 能水解 |
| D | C4H10O | 有3个甲基的醇 |
| A. | A | B. | B | C. | C | D. | D |

 具有水果香味的中性物质A可以发生下列变化:
具有水果香味的中性物质A可以发生下列变化: