题目内容
16.在一定温度下,向一个2L的真空密闭容器中(预先装入催化剂)通入1mol N2和3mol H2,经过一段时间后,测得容器内压强与起始时的压强之比为9:10.在此时间内H2的平均反应速率为0.1mol•(L•min)-1,则经过时间为( )| A. | 2 min | B. | 3 min | C. | 4 min | D. | 5 min |
分析 恒温恒容条件下,气体压强之比等于物质的量之比,依据化学平衡三行计算得到氢气消耗的浓度,结合v=$\frac{△c}{△t}$计算反应时间.
解答 解:在一定温度下,向一个2L的真空密闭容器中(预先装入催化剂)通入1mol N2和3mol H2,设反应中消耗氮气物质的量为x,N2+3H2=2NH3,
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
一段时间(mol) 1-x 3-3x 2x
经过一段时间后,测得容器内压强与起始时的压强之比为9:10,恒温恒容条件下,气体压强之比等于物质的量之比,、
( 1-x+3-3x+2x):(1+3)=9:10
x=0.2mol,
氢气消耗浓度c(H2)=$\frac{3×0.2mol}{2L}$=0.3mol/L,
则经过时间=$\frac{0.3mol/L}{0.1mol/(L•min)}$=3min,
故选B.
点评 本题考查了化学反应速率概念理解和计算应用,注意一定条件下气体物质的量之比等于气体压强之比,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
6.NA为阿佛加德罗常数,下述正确的是( )
| A. | 12 kg12C含有NA个碳原子 | |
| B. | 1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA | |
| C. | 标准状况下,11.2L四氯化碳所含分子数为0.5 NA | |
| D. | 在铁与硫的反应中,1mol铁失去的电子数为2 NA |
7.同位素示踪法可用于反应机理的研究,下列反应中同位素示踪表示正确的是( )
| A. | CH3COOH+CH3CH218OH═CH3COOCH2CH3+H218O | |
| B. | K37ClO3+6HCl═K37Cl+3Cl2↑+3H2O | |
| C. | 2Na218O2+2H2O═4Nal8OH+O2↑ | |
| D. | 2KMnO4+5H218O2+3H2SO4═K2SO4+2MnSO4+518O2↑+8H2O |
4.某有机化合物的结构简式如图所示,关于该化合物的下列说法正确的是( )


| A. | 由于含有氧元素不是有机物 | |
| B. | 完全燃烧时只有二氧化碳和水两种产物 | |
| C. | 属于醇 | |
| D. | 不能使溴水褪色 |
11.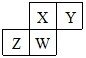 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
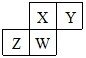 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )
短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子数的三倍,下列说法错误的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 元素X、Y、Z、W的最高化合价分别与其主族序数相等 | |
| C. | 最简单气态氢化物的热稳定性:Y>X>W>Z | |
| D. | 最高价氧化物对应水化物的酸性:X>W>Z |
1.下面的烷烃是烯烃R和氢气发生加成反应后的产物,则R可能的结构简式有( )
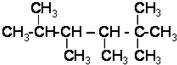

| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
8.下列说法正确的是( )
| A. | 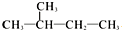 与 与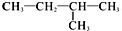 互为同分异构体 互为同分异构体 | |
| B. | CH3-CH2-CH3、CH3-CH2-CH2-CH2-CH3、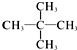 互为同系物,熔沸点逐渐升高 互为同系物,熔沸点逐渐升高 | |
| C. | 烷烃燃烧通式为:CnH2n+2+$\frac{3n+1}{2}$O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O | |
| D. | 分子式为C4H10O并能与金属钠反应放出氢气的有机物有3种 |
 具有水果香味的中性物质A可以发生下列变化:
具有水果香味的中性物质A可以发生下列变化: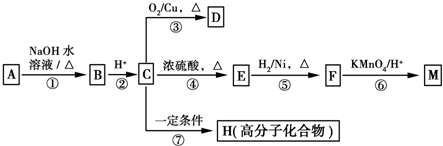
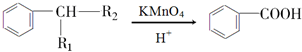 (R1、R2表示烃基或氢原子)
(R1、R2表示烃基或氢原子)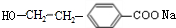 .
.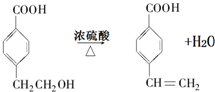 .
. .
.