题目内容
12.某烃蒸气的密度是相同状况下H2密度的34倍,求该烃分子式.分析 某烃蒸气的密度是相同状况下H2密度的34倍,则相对分子质量为34×2=68,利用商余法计算烃的分子式.
解答 解:某烃蒸气的密度是相同状况下H2密度的34倍,则相对分子质量为34×2=68,则68÷12=5…8,则分子式为C5H8,
答;该烃的分子式为C5H8.
点评 本题考查有机物分子式的确定的计算,为高频考点,题目难度不大,注意掌握商余法在化学计算中的应用方法,试题培养了学生的化学计算能力.

练习册系列答案
相关题目
3.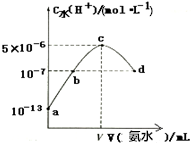 常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )
常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )
 常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )
常温下,向20mL某浓度的硫酸中滴入0.1mol•L-1氨水,溶液中水电离出的氢离子浓度随加入氨水的体积变化如图所示.下列分析正确是( )| A. | 该硫酸的浓度为1mol•L-1 | |
| B. | b点所示溶液中:c(NH4+)=2c(SO42-) | |
| C. | V=40 | |
| D. | c点所示溶液中:c(H+)-c(OH-)═c(NH3•H2O) |
20.下列烃的名称中正确的是( )
| A. | 2-甲基-2-乙基戊烷 | B. | 3-甲基--己烯 | ||
| C. | 2-甲基-4-庚炔 | D. | 1,2,4-三甲苯 |
7.某溶液中Cl-、Br-、I-的物质的量之比为2:3:4.要使溶液中的Cl-、Br-、I-离子数之比变为4:3:2,则通入Cl2的分子数是原溶液中I-离子个数的( )
| A. | $\frac{1}{2}$ | B. | $\frac{1}{3}$ | C. | $\frac{1}{4}$ | D. | $\frac{1}{5}$ |
4.在恒温恒容密闭容器中充入0.5molN2和1.5molH2发生反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol充分反应后,下列说法正确的是( )
| A. | 在和上面初始体积相同的恒温恒压密闭容器中,也充入0.5molN2和1.5molH2发生反应则达到平衡时,放出的热量大于46.2kJ | |
| B. | 在平衡时再充入1molNH3则平衡向左移动,则平衡时N2的百分含量减小 | |
| C. | 若向容器中充入一定量He气,则平衡向右移动 | |
| D. | 在平衡后再充入1molH2,则N2的转化率增大,且平衡常数增大 |
1.常温下列各组离子在指定溶液中可能大量共存的是( )
| A. | 能使淀粉碘化钾试纸显蓝色的溶液:Na+、H+、I-、SO32- | |
| B. | 饱和CO2的溶液中:Ca2+、K+、NO3-、Cl- | |
| C. | 在pH=14的溶液中:Na+、K+、Cl-、SO2 | |
| D. | 无色透明溶液:Na+、Ba2+、MnO4-、Cl- |
5.下列化合物,苯环上的氢原子被澳原子取代,所得一溴代物有三种同分异构体的是( )

| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
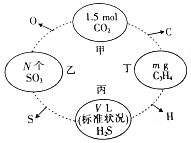 如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)
如图,两相邻圆圈内物质间含有相同的某一原子,且该原子的物质的量相同.(设NA为阿伏伽德罗常数的值)