题目内容
19.下列变化过程,属于吸热过程的是( )①液态水变成水蒸气
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤CH3COONa水解
⑥CH3COOH电离.
| A. | ②③④⑤ | B. | ②③④ | C. | ②⑤ | D. | ①⑤⑥ |
分析 根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱).
解答 解:①液态水变成水蒸气要吸热,属于吸热过程,故正确;
②酸碱中和反应是放热反应,故错误;
③浓H2SO4稀释是放热过程,故错误;
④固体NaOH溶于水放出大量的热,是放热过程,故错误;
⑤盐类的水解是酸碱中和的逆反应,故为吸热反应,故CH3COONa水解属于吸热过程,故正确;
⑥弱电解质的电离是吸热过程,故CH3COOH电离要吸热,故正确.
故选D.
点评 本题考查吸热反应,题目难度不大,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆.

练习册系列答案
相关题目
9.NA表示阿伏加德罗常数,下列说法不正确的是( )
| A. | H2SO4的摩尔质量(kg/mol)与NA个硫酸分子的质量(g)在数值上相等 | |
| B. | NA个氧气分子和NA个氮气分子的质量比为8:7 | |
| C. | 1.5 L 0.3 mol•L-1Na2SO4溶液中含0.9NA个Na+ | |
| D. | 非标准状况下,22.4LO2中含有氧分子可能为NA个 |
10.关于实验事故或药品的处理方法中,正确的是( )
| A. | 少量浓硫酸沾在皮肤上,立即用大量氢氧化钠溶液冲洗 | |
| B. | 制取蒸馏水时,为了防止瓶内产生暴沸现象,应先向烧瓶内加几片碎瓷片 | |
| C. | 配制稀硫酸时,可先在量筒中加一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 不慎洒出的酒精在桌上着火时,应立即用大量水扑灭 |
14.下列说法中,正确的一项是( )
| A. | 氯化钠溶液是电解质 | |
| B. | 因为醋酸是弱电解质,所以醋酸在熔融状态下和在溶液中都不能导电 | |
| C. | 在氢气还原氧化铜的实验中,氢气是氧化剂 | |
| D. | 胶体的本质特征是粒子大小在1nm-100nm之间 |
4.已知反应CO(g)═C(s)+1/2O2(g)的△H为正值,△S为负值.若△H和△S随温度的变化忽略不计,下列说法中正确的是( )
| A. | 低温下反应是自发进行,高温下反应是非自发进行 | |
| B. | 任何温度下反应都是自发进行 | |
| C. | 低温下反应是非自发进行,高温下反应是自发进行 | |
| D. | 任何温度下反应都是非自发进行 |
11.现有等浓度的下列物质的溶液:①CH3COOH ②HClO ③NaClO ④H2CO3 ⑤Na2CO3 ⑥NaHCO3.按溶液pH由小到大排列正确的是( )
| A. | ④①②⑤⑥③ | B. | ④①②⑥⑤③ | C. | ①④②⑥③⑤ | D. | ①④②③⑥⑤ |
8.在[Pb2+]为0.200mol/L的溶液中,若每升加入0.201mol的Na2SO4(设条件不变),留在溶液中的Pb2+的百分率是(已知PbSO4的Ksp=1.8×10-8)( )
| A. | 1×10-3% | B. | 2×10-4% | C. | 9×10-3% | D. | 2.5×10-20% |
9. 容器中发生一化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )
容器中发生一化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )
 容器中发生一化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )
容器中发生一化学反应,反应过程中存在H2O、ClO-、CN-、HCO3-、N2、Cl-六种物质,在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示.下列有关判断中正确的是( )| A. | 还原剂是含CN-的物质,氧化产物只有N2 | |
| B. | 氧化剂是ClO-,还原产物是HCO3- | |
| C. | 氧化剂与还原剂的化学计量数之比为5:2 | |
| D. | 若生成2.24LN2,则转移电子必定为1mol |
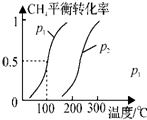 甲醇是一种重要的化工原料,在生产中有着重要的应用.工业上用天然气为原料,分为两阶段制备甲醇:
甲醇是一种重要的化工原料,在生产中有着重要的应用.工业上用天然气为原料,分为两阶段制备甲醇: