题目内容
下列各组混合物中,可以直接用分液漏斗分离的是( )
| A、酒精和碘 | B、苯酚和乙醇 |
| C、乙醇和水 | D、溴乙烷和水 |
考点:分液和萃取
专题:化学实验基本操作
分析:根据分液漏斗可以将互不相溶的两层液体分开,则分析选项中物质的溶解性即可.
解答:
解:A.酒精和碘能互溶,所以不能用分液漏斗分离,故A错误;
B.苯酚和乙醇都是有机物能互溶,所以不能用分液漏斗分离,故B错误;
C.乙醇和水能互溶,所以不能用分液漏斗分离,故C错误;
D.溴乙烷和水不互溶,出现分层,所以能用分液漏斗分离,故D正确.
故选D.
B.苯酚和乙醇都是有机物能互溶,所以不能用分液漏斗分离,故B错误;
C.乙醇和水能互溶,所以不能用分液漏斗分离,故C错误;
D.溴乙烷和水不互溶,出现分层,所以能用分液漏斗分离,故D正确.
故选D.
点评:本题考查物质的分离,题目难度不大,本题注意把握常见混合物的分离原理、方法以及操作的注意事项等.

练习册系列答案
相关题目
下列物质在空气中露置容易变质的是( )
| A、NaCl |
| B、CaCO3 |
| C、NaOH |
| D、KNO3 |
下列说法正确的是( )
| A、CO、NO、NO2 都是大气污染气体,在空气中都能稳定存在 |
| B、1mol Cu和足量稀硝酸反应产生NA个NO分子(NA为阿伏加德罗常数) |
| C、pH=1的溶液中,Fe2+、NO3-、SO42-、Na+不能大量共存 |
| D、铁溶于稀HNO3,溶液变黄,发生离子反应为3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
在两个容积相同的容器中,一个盛有NO气体,另一个盛有N2和O2的混合气体,在同温同压下,两容器内的气体一定具有相同的( )
| A、原子数 | B、密度 |
| C、质量 | D、摩尔质量 |
下列叙述正确的是( )
| A、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B、含1mol Ba(OH)2的稀溶液和含1 mol H2SO4的稀溶液反应释放热量akJ,则表示该反应中和热的热化学反应方程式为:OH-(aq)+H+(aq)=H2O(l)H=-a kJ?mol-1 |
| C、电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的Cl2进入阳极室 |
| D、向Ba(OH)2溶液中加入足量的NaHCO3溶液:Ba2++2OH-+2HCO3-=BaCO3↓+CO32-+2H2O |
下列装置或操作能达到实验目的是( )
A、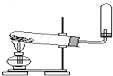 制备收集NH3 |
B、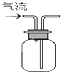 收集CO2气体 |
C、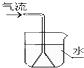 溶解吸收NH3 |
D、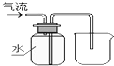 收集NO气体 |
最近,科学家冶炼出纯度高达99.999%的铝,你估计它具有性质是( )
| A、熔点比铁铝合金小 |
| B、在冷、浓HNO3中可以钝化 |
| C、在空气中放置容易生锈,进而被腐蚀 |
| D、当它与铁的粉碎粒度相同时,与4mol/L盐酸反应速率比纯铁大 |
用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A、标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
| B、标准状况下,14 g氮气含有的核外电子数为5NA |
| C、由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
| D、NA个一氧化碳分子和0.5 mol 甲烷的质量比为7:4 |
A、B、C、D、E为原子序数依次增大的短周期元素.已知A的一种单质是自然界中最硬的物质,B与D同主族,C与E同主族,B的一种单质能用于自来水消毒,C在元素周期表中的非金属性最强.则下列说法正确的是( )
| A、C的最高价氧化物对应的水化物的酸性最强 |
| B、最简单气态氢化物的稳定性E>D>B |
| C、A与B形成的化合物在反应中只能作还原剂 |
| D、A分别与其他四种元素形成的化合物一定是共价化台物 |