题目内容
16.下列叙述正确的是( )| A. | 增大反应物浓度能增大有效碰撞的几率 | |
| B. | 增加压强能增大反应物活化分子的百分数 | |
| C. | 增加反应物浓度能增大反应物活化分子的百分数 | |
| D. | 分解反应都是吸热反应 |
分析 活化分子发生反应生成新物质的碰撞为有效碰撞,增大浓度、压强,可增大单位体积活化分子数目,升高温度、加入催化剂,可增大活化分子数目,进而增大反应速率,以此解答该题.
解答 解:A、增大反应物浓度,单位体积内活化分子数增多,增大有效碰撞的几率,可增大反应速率,故A正确;
B、对于有气体参加的反应,增大压强,反应速率加快,活化分子数目增大,但百分数不变,故B错误;
C、加浓度,反应速率加快,活化分子数目增大,但百分数不变,故C错误;
D、反应2H2O2=2H20+O2为分解反应,该反应为放热反应,所以分解反应不一定为吸热反应,故D错误;
故选A.
点评 本题考查温度、浓度、催化剂对反应速率的影响,题目难度不大,注意对活化分子的浓度以及百分数的影响.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.下列除杂方案设计错误的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A | Fe | Al | NaOH溶液 | 过滤 |
| B | 乙酸乙酯 | 乙醇 | 水 | 水洗、分液 |
| C | CO2 | SO2 | 饱和NaHCO3溶液、浓H2SO4 | 洗气 |
| D | NH4Cl(aq) | Cu2+(aq) | NaOH溶液 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
11.下列说法正确的是( )
| A. | 合成氨反应中为了提高正反应速率,及时抽走氨气 | |
| B. | SO2催化氧化中通入过量空气可提高SO2的平衡转化率 | |
| C. | 合成氨中加入催化剂可提高氮气的平衡转化率 | |
| D. | 合成氨反应中缩小容器体积可以使平衡正向移动,所以氮气浓度减小 |
1.相同状况下,等质量的下列物质中,体积最大的是( )
| A. | O2 | B. | HCl | C. | CO2 | D. | NH3 |
5.在2A+B═3C+4D反应中,表示该反应速率最快的数据是( )
| A. | v(A)=0.5 mol•L-1•s-1 | B. | v(B)=0.3 mol•L-1•s-1 | ||
| C. | v(C)=0.8 mol•L-1•s-1 | D. | v(D)=1.0 mol•L-1•s-1 |
6.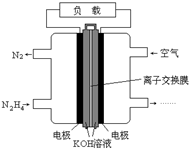 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
 液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )
液体燃料电池相比于气体燃料电池具有体积小,无需气体存储装置等优点.一种以肼(N2H4)为燃料的电池装置如图所示.该电池用空气中的氧气作为氧化剂,KOH作为电解质.下列关于该燃料电池的叙述正确的是( )| A. | 电子从右侧电极经过负载后流向左侧电极 | |
| B. | 负极发生的电极反应式为:N2H4-4e-=N2+4H+ | |
| C. | 该燃料电池的电极材料应采用多孔导电材料,以提高电极反应物质在电极表面的吸附量,并使它们与电解质溶液充分接触 | |
| D. | 该燃料电池持续放电时.K+从负极向正极迁移,因而离子交换膜需选用阳离子交换膜 |
 .
. .
.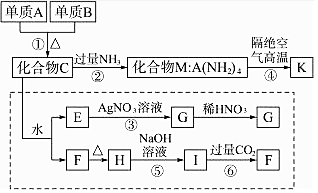 材料科学是近年来与化学有关的科学研究的重点,某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化等特性,它是以中学化学中的常见物质为原料来生产的.如图所示为其生产过程,其中虚线框内转化是为探究C的组成而设.已知A、B均为非金属单质,G、F、H均难溶于水且为白色粉末;图中除M、K(均含A元素)外均为中学化学常见物质:
材料科学是近年来与化学有关的科学研究的重点,某新型无机非金属材料K由两种非金属元素组成,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化等特性,它是以中学化学中的常见物质为原料来生产的.如图所示为其生产过程,其中虚线框内转化是为探究C的组成而设.已知A、B均为非金属单质,G、F、H均难溶于水且为白色粉末;图中除M、K(均含A元素)外均为中学化学常见物质: