题目内容
4.铅蓄电池是典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42- $?_{充电}^{放电}$2PbSO4+2H2O,请回答下列问题:(1)放电时,负极材料是Pb,电解液中H2SO4的浓度将变小(“变大”、“变小”或“不变”);
(2)充电时,阴极的电极反应式是PbSO4+2e-=Pb+SO42-.
分析 依据铅蓄电池的电池总反应式分析,放电为原电池,充电为电解池,依据反应的总电池反应,结合元素化合价变化分析,原电池反应中Pb元素化合价升高的在负极失电子发生氧化反应,PbO2中元素化合价降低的是在正极得到电子发生还原反应生成硫酸铅,充电过程中原电池的负极连接电源负极做电解池的阴极发生还原反应,原电池正极和电源正极连接做电解池的阳极发生氧化反应,据此分析解答.
解答 解;(1)铅蓄电池的电池总反应式为:Pb+PbO2+4H++2SO42- $?_{充电}^{放电}$2PbSO4+2H2O;放电为原电池,依据反应的总电池反应,结合元素化合价变化分析,原电池反应中Pb元素化合价升高的在负极失电子发生氧化反应,PbO2中元素化合价降低的是在正极得到电子发生还原反应生成硫酸铅,反应消耗硫酸,所以电解液中H2SO4的浓度将变小,故答案为:Pb;变小;
(2)充电过程中原电池的负极连接电源负极做电解池的阴极发生还原反应,电极反应为:PbSO4+2e-=Pb+SO42-,故答案为:PbSO4+2e-=Pb+SO42-.
点评 本题考查了原电池和电解池原理的分析应用,主要是电极反应书写是解题关键,题目较简单.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
14.下列说法中正确的是( )
| A. | 3p2表示3p能级有两个轨道 | |
| B. | 同一原子中,1s、2s、3s电子能量逐渐减小 | |
| C. | 处于最低能量的原子叫做基态原子 | |
| D. | 同一原子中,2p、3p、4p能级的轨道数依次增多 |
12.下列不属于油脂的是( )
①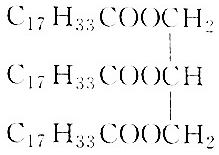 ②
②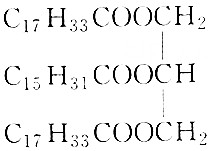 ③
③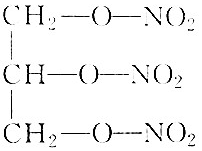 ④花生油⑤润滑油⑥石蜡⑦菜油.
④花生油⑤润滑油⑥石蜡⑦菜油.
①
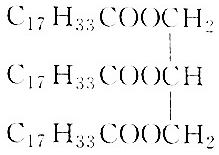 ②
②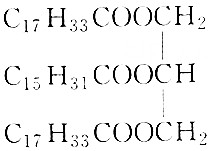 ③
③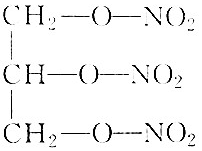 ④花生油⑤润滑油⑥石蜡⑦菜油.
④花生油⑤润滑油⑥石蜡⑦菜油.| A. | ①②③④⑦ | B. | ①②④⑦ | C. | ①②③④⑤⑥⑦ | D. | ③⑤⑥ |
19.下列事实中,不能用平衡移动原理解释的是( )
| A. | 氯气中有下列平衡Cl2+H2O?HCl+HClO,当加入AgNO3(s)后溶液颜色变浅 | |
| B. | 2NO2(g)?N2O4(g)△H<0,升高温度可使体系颜色加深 | |
| C. | 反应CO+NO2?CO2+NO△H<0,升高温度可使平衡向逆反应方向移动 | |
| D. | 合成氨反应N2+3H2?2NH3△H<0,使用催化剂加快反应速率 |
9.除去下列物质中的杂质,所用试剂和方法不正确的是( )
| 物质 | 杂质 | 除杂质所用试剂和方法 | |
| A | KCl溶液 | I2 | CCl4,萃取 |
| B | KNO3 | K2SO4 | Ba(NO3)2溶液,过滤 |
| C | Cu | CuO | 盐酸,过滤 |
| D | CaCO3 | CaO | 盐酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.一定条件下,利用如图所示装置可实现有机物的储氢,下列有关说法不正确的是( )


| A. | 电源A为负极,电极C为阳极 | |
| B. | 单一气体为O2 | |
| C. | 该储氢装置的电流效率约为64.3%(电流效率计算公式为:=$\frac{生成目标产物消耗的电子数}{转移的电子数}$×100%) | |
| D. | 导线中电子流动方向为:A→D→C→B |
13.下列说法正确的是( )
| A. | 加碘盐的溶液遇淀粉变蓝 | |
| B. | CaO 不可用作工业废气的脱硫剂 | |
| C. | 二氧化硫可作纸浆的漂白剂 | |
| D. | 纳米铁粉可以高效地去除被污染水体中的 Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其 本质是纳米铁粉对重金属离子较强的物理吸附 |
14.下列溶液中的c (Cl -)与100mL 1mol•L-1氯化铝溶液中的c (Cl-)相等( )
| A. | 300mL 1mol•L-1 氯化钠溶液 | B. | 150mL 2mol•L-1氯化铵溶液 | ||
| C. | 75mL 3mol•L-1 氯化钙溶液 | D. | 10mL 1.5mol•L-1 氯化钡溶液 |
 辣条是深受中小学生喜爱的小零食,并且已走出国门,畅销海外,右图是某品牌辣条产品标签的一部分.
辣条是深受中小学生喜爱的小零食,并且已走出国门,畅销海外,右图是某品牌辣条产品标签的一部分.