题目内容
利用如图所示装置,设计一个简单的一次性完成的实验,验证乙酸、碳酸和苯酚的酸性强弱.

(1)用导管口的字母表示所选用装置的连接顺序: .
(2)装置A中,广口瓶中所放入的物质是,分液漏斗中所放入的物质是 .
(3)装置B中所加入的物质是,其作用是 .
(4)装置C中反应的离子方程式为 .

(1)用导管口的字母表示所选用装置的连接顺序:
(2)装置A中,广口瓶中所放入的物质是,分液漏斗中所放入的物质是
(3)装置B中所加入的物质是,其作用是
(4)装置C中反应的离子方程式为
考点:比较弱酸的相对强弱的实验
专题:实验题
分析:(1)根据乙酸酸性大于醋酸、醋酸酸性大于苯酚进行连接装置;
(2)装置A用于证明醋酸酸性大于碳酸,反应物为碳酸盐和醋酸,据此进行解答;
(3)醋酸具有挥发性,所以需要将二氧化碳中混有的醋酸除掉,避免乙酸与苯酚钠溶液反应;
(4)装置C中证明碳酸酸性大于苯酚,发生的反应为二氧化碳与苯酚钠的溶液的反应,据此写出反应的离子方程式.
(2)装置A用于证明醋酸酸性大于碳酸,反应物为碳酸盐和醋酸,据此进行解答;
(3)醋酸具有挥发性,所以需要将二氧化碳中混有的醋酸除掉,避免乙酸与苯酚钠溶液反应;
(4)装置C中证明碳酸酸性大于苯酚,发生的反应为二氧化碳与苯酚钠的溶液的反应,据此写出反应的离子方程式.
解答:
解:(1)乙酸能和碳酸盐反应生成CO2,而CO2气体通入苯酚钠溶液中又有苯酚生成,所以正确的连接顺序是a→c→b→d,
故答案为:a→c→b→d;
(2)根据以上分析可知,装置A中,广口瓶中所放入的物质是CaCO3或 Na2CO3,分液漏斗中所放入的物质是CH3COOH溶液,
故答案为:CaCO3或 Na2CO3; CH3COOH溶液;
(3)由于乙酸易挥发,且乙酸也能和苯酚钠反应,所以装置B中所加入的物质是碳酸氢钠,其作用是吸收挥发出来的乙酸,避免乙酸与苯酚钠溶液反应,
故答案为:NaHCO3溶液,吸收挥发出来的乙酸,避免乙酸与苯酚钠溶液反应;
(4)装置C中苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠,反应的离子方程式为:H2O+CO2+C6H5O-→C6H5OH+HCO3-,
故答案为:H2O+CO2+C6H5O-→C6H5OH+HCO3-.
故答案为:a→c→b→d;
(2)根据以上分析可知,装置A中,广口瓶中所放入的物质是CaCO3或 Na2CO3,分液漏斗中所放入的物质是CH3COOH溶液,
故答案为:CaCO3或 Na2CO3; CH3COOH溶液;
(3)由于乙酸易挥发,且乙酸也能和苯酚钠反应,所以装置B中所加入的物质是碳酸氢钠,其作用是吸收挥发出来的乙酸,避免乙酸与苯酚钠溶液反应,
故答案为:NaHCO3溶液,吸收挥发出来的乙酸,避免乙酸与苯酚钠溶液反应;
(4)装置C中苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠,反应的离子方程式为:H2O+CO2+C6H5O-→C6H5OH+HCO3-,
故答案为:H2O+CO2+C6H5O-→C6H5OH+HCO3-.
点评:本题考查乙酸、碳酸、苯酚酸性强弱比较以及实验设计、除杂及方程式的书写,该题是中等难度的试题,试题注重基础,侧重考查学生分析问题、解决问题的能力;该题只要是要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论,有助于培养学生的逻辑思维能力和创新思维能力.

练习册系列答案
相关题目
下列反应的离子方程式书写不正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、氧化亚铁溶于稀盐酸:FeO+2H+=Fe2++H2O |
| C、二氧化硅与烧碱溶液反应:SiO2+2OH-=SiO32-+H2O |
| D、除去氧化膜的铝片插入硝酸汞溶液中:2Al+3Hg2+=2Al3++3Hg |
下列叙述正确的是( )


| A、K与N连接时,X为硫酸,一段时间后溶液的pH减小 |
| B、K与N连接时,X为氯化钠,石墨电极反应:2H++2e-=H2↑ |
| C、K与M连接时,X为氯化钠,石墨电极反应:4OH--4e-=2H2O+O2↑ |
| D、K与M连接时,X为硫酸,一段时间后溶液的pH减小 |
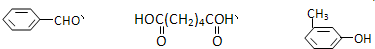
 互为同分异构体的是
互为同分异构体的是 已知:A、B、C、D、E、G、L七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;L原子核外最外层电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、G的原子均有三个能层,C原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;C与G能形成原子数目比为1:3、熔点为190℃的化合物Q.
已知:A、B、C、D、E、G、L七种元素的核电荷数依次增大,属于元素周期表中前四周期的元素.其中A原子在基态时p轨道半充满且电负性是同族元素中最大的;D、E原子核外的M层中均有两个未成对电子;L原子核外最外层电子数与B相同,其余各层均充满.B、E两元素组成化合物B2E的晶体为离子晶体.C、G的原子均有三个能层,C原子的第一至第四电离能(kJ/mol)分别为:578、1817、2745、ll575;C与G能形成原子数目比为1:3、熔点为190℃的化合物Q.