题目内容
8. 苹果酸是一种常见的有机酸,其结构简式如图.苹果酸可能发生的反应是( )
苹果酸是一种常见的有机酸,其结构简式如图.苹果酸可能发生的反应是( )①与NaOH溶液反应 ②使石蕊溶液变红 ③与金属钠反应放出气体
④一定条件下与乙酸发生酯化反应 ⑤一定条件下与乙醇发生酯化反应.
| A. | ①②③ | B. | ①②③④ | C. | ①②③⑤ | D. | ①②③④⑤ |
分析 由结构简式可知,分子中含-COOH、-OH,结合羧酸、醇的性质来解答.
解答 解:①苹果酸中含有羧基,有酸性,可与NaOH溶液反应,故①正确;
②苹果酸中含有羧基,有酸性,可以与石蕊试液作用变红,故②正确;
③苹果酸中含有羧基和羟基,均可以与金属钠反应放出氢气,故③正确;
④苹果酸中含有羟基,一定条件下与乙酸酯化,故④正确;
⑤苹果酸中含有羧基,一定条件下与乙醇酯化,故⑤正确;
故选D.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意羧酸、醇的性质,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
19.已知某有机物中n(C):n(H)=1:1,取W1g该有机物在足量氧气中充分燃烧,消耗标准状况下的氧气VL,产物只有CO2和H2O,且m(CO2)=W2g,m(H2O)=W3g.
(1)符合n(C):n(H)=1:1的最简单的有机物:
①若是烃,则结构简式为CH≡CH;②若是烃的含氧衍生物,则结构式为OHCCHO.
(2)当W1与V之间满足W1=$\frac{13V}{28}$条件时,该有机物中一定没有氧原子.当W1与V之间满足W1<$\frac{13V}{28}$条件时,该有机物中一定有氧原子.若该有机物含有氧元素,则W1g有机物中含氧的质量为W1-$\frac{13W{\;}_{2}}{44}$g(用含Wl、W2的代数式表示).
(3)若通过计算来确定该有机物是否含氧,除已知的碳氢原子个数比外还至少需上述数据中的2个,将这些组合一一填入下列空格中.
说明:①选用V、W1、W2、W3表示,不必列出具体计算式.
②每个空格中填一种组合,有几种组合就填几种,不一定填满.
(4)如果符合n(C):n(H)=1:1的有机物在氧气不足时燃烧,生成CO、CO2和水蒸气的混合气体共3mol,将混合气体通入盛有足量Na2O2的密闭容器中,用电火花引燃直到反应完全,则剩余气体的物质的量(n)的范围为0.5mol<n(O2)<1.5mol.(写出计算过程)
【已知:CO不与Na2O2反应,2CO2+2Na2O2→2Na2CO3+O2↑; 2H2O+2Na2O2→4NaOH+O2↑】
(1)符合n(C):n(H)=1:1的最简单的有机物:
①若是烃,则结构简式为CH≡CH;②若是烃的含氧衍生物,则结构式为OHCCHO.
(2)当W1与V之间满足W1=$\frac{13V}{28}$条件时,该有机物中一定没有氧原子.当W1与V之间满足W1<$\frac{13V}{28}$条件时,该有机物中一定有氧原子.若该有机物含有氧元素,则W1g有机物中含氧的质量为W1-$\frac{13W{\;}_{2}}{44}$g(用含Wl、W2的代数式表示).
(3)若通过计算来确定该有机物是否含氧,除已知的碳氢原子个数比外还至少需上述数据中的2个,将这些组合一一填入下列空格中.
说明:①选用V、W1、W2、W3表示,不必列出具体计算式.
②每个空格中填一种组合,有几种组合就填几种,不一定填满.
| 组合序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ | Ⅴ | Ⅵ |
| 组合数据 |
【已知:CO不与Na2O2反应,2CO2+2Na2O2→2Na2CO3+O2↑; 2H2O+2Na2O2→4NaOH+O2↑】
16.某同学进行试验探究时,欲配制1.0molL-1Ba(OH)2溶液,但只找到在空气中暴露已久的Ba(OH)2•8H2O试剂(化学式量:315).在室温下配制溶液时发现所取试剂在水中仅部分溶解,烧杯中存在大量未溶物.
为探究原因,该同学查得Ba(OH)2•8H2O 部分溶解度数据,见下表:
(1)烧杯中未溶物仅为BaCO3,理由是Ba(OH)2•8H2O与CO2作用转化为BaCO3.
(2)假设试剂由大量Ba(OH)2•8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题纸上写出实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
(3)将试剂初步提纯后,准确测定其中Ba(OH)2•8H2O的含量.
实验如下:①配制250mL 约0.1mol•L-1Ba(OH)2•8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,搅拌,将溶液转入250ml的容量瓶中,洗涤,定容,摇匀.
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将0.1980 (填“0.020”、“0.05”、“0.1980”或“1.5”)molL-1盐酸装入50ml酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸Vml.
(4)室温下,不能(填“能”或“不能”) 配制1.0mol•L-1Ba(OH)2溶液,说明理由室温下,氢氧化钡的溶解度为3.9g,溶液的物质的量浓度约是$\frac{\frac{3.9g}{171g/mol}}{0.1L}$=0.23mol/L<1.0mol•L-1.
为探究原因,该同学查得Ba(OH)2•8H2O 部分溶解度数据,见下表:
| 温度 | 283K | 293K | 303K |
| 溶解度(g/100g H2O) | 2.5 | 3.9 | 5.6 |
(2)假设试剂由大量Ba(OH)2•8H2O和少量BaCO3组成,设计试验方案,进行成分检验,在答题纸上写出实验步骤、预期现象和结论.(不考虑结晶水的检验;室温时BaCO3饱和溶液的pH=9.6)
限选试剂及仪器:稀盐酸、稀硫酸、NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置,过滤,得滤液和沉淀. | |
| 步骤2:取适量滤液于试管中,滴加稀硫酸. | 出现白色沉淀,说明该试剂中有Ba2+存在 |
| 步骤3:取适量步骤1中的沉淀于试管中,滴加稀盐酸连接带塞导气管将产生的气体导入澄清石灰水中. | 澄清石灰水变混浊.说明该试剂中含有BaCO3 |
| 步骤4:取步骤1中的滤液于烧杯中,用pH计测其pH值 | pH值明显大于9.6,说明该试剂中含有Ba(OH)2. |
实验如下:①配制250mL 约0.1mol•L-1Ba(OH)2•8H2O溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水,搅拌,将溶液转入250ml的容量瓶中,洗涤,定容,摇匀.
②滴定:准确量取25.00ml所配制Ba(OH)2溶液于锥形瓶中,滴加指示剂,将0.1980 (填“0.020”、“0.05”、“0.1980”或“1.5”)molL-1盐酸装入50ml酸式滴定管,滴定至终点,记录数据.重复滴定2次.平均消耗盐酸Vml.
(4)室温下,不能(填“能”或“不能”) 配制1.0mol•L-1Ba(OH)2溶液,说明理由室温下,氢氧化钡的溶解度为3.9g,溶液的物质的量浓度约是$\frac{\frac{3.9g}{171g/mol}}{0.1L}$=0.23mol/L<1.0mol•L-1.
3.反应A(g)+3B(g)?2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.04mol/(L•s) | ||
| C. | v(C)=0.03mol/(L•s) | D. | v(D)=0.4mol/(L•min) |
17.通常情况下能共存且能用浓硫酸干燥的一组气体是( )
| A. | SO2、Cl2、H2S | B. | O2、H2、SO2 | C. | CH4、HCl、NH3 | D. | NO、SO3、O2 |
18.进入21世纪以来,世界各国对于开发新能源的举措越来越新奇,下列做法不可行的是( )
| A. | 美国一些科学家开发利用人体能,一些超级市场将顾客拉门消耗的能量贮存起来转化为电能,用于超级市场的电能消耗 | |
| B. | 英国农村大面积种植油菜,用植物油代替石油 | |
| C. | 英国科学家对一种嗜热链球菌进行基因移植后,新繁殖后的大量细菌在较高温度下,把稻草中的植物纤维转变为乙醇 | |
| D. | 英美科学家在酶的作用下将水分解成氢气和氧气,利用其释放的能量 |
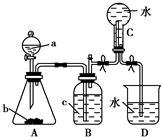 如图装置是某种气体X的制取装置和收集装置(必要时可加热).所用的试剂从下列试剂中选取2~3种:硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水.请回答下列问题:
如图装置是某种气体X的制取装置和收集装置(必要时可加热).所用的试剂从下列试剂中选取2~3种:硫化亚铁、二氧化锰、铜屑、氯化铵、稀硝酸、浓盐酸、蒸馏水.请回答下列问题: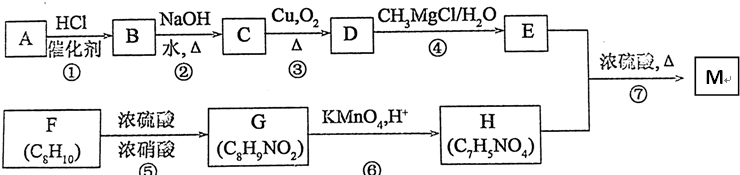
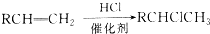
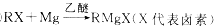
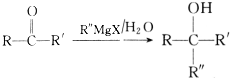
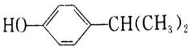
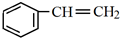 ,C中官能团的名称为羟基.
,C中官能团的名称为羟基.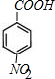 +
+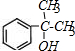 $?_{△}^{浓硫酸}$
$?_{△}^{浓硫酸}$ +H2O.
+H2O. 、
、 .
.