��Ŀ����
1��NaCl��һ�ֻ�������ԭ�ϣ�ͨ����ⱥ��ʳ��ˮ�����Ƶ�NaOH��H2��Cl2�����������գ���1��д����ⱥ��ʳ��ˮ�Ļ�ѧ����ʽ2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2����
��2����ԭ�ӵ����������Ų�ʽΪ3S23P5�������Ӻ�����18���˶�״̬��ͬ�ĵ��ӣ�
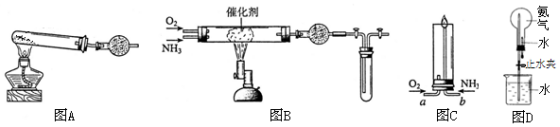
��3������ѹ����ΪҺ�����������仯��ѡ�����������ѧ����������Ũ��ˮ��������ȹܵ��Ƿ�й©��й©����۲쵽�����İ��̣�NH4Cl����������һ����ɫ��ζ�ĵ������壬д���˷�Ӧ�Ļ�ѧ����ʽ���������ת�Ƶķ������Ŀ
 ��
����4�������������궨��ˮ�еⵥ�ʵĺ�����5Cl2+I2+6H2O��10HCl+2HIO3���ⶨʱ��������������ȷ����������������Ե�����ָʾ����ָʾ��Ӧ�յ㣬��Ӧ�յ�ʱ����������Һ����ɫ��Ϊ��ɫ�����ڰ�����ڲ���ɫ��
�������궨һ�������ˮ�еⵥ�ʵ�Ũ�ȣ���������ƽ��ʵ�飬���ݼ�¼������
| ��ˮ�������mL�� | ����������������mL�� |
| 500 | 56 |
| 500 | 55 |
| 500 | 57 |
���� ��1����ⱥ��ʳ��ˮ�����������ɡ�������������
��2����ԭ�Ӻ��������Ϊ17�������������ԭ����д���������Ų�ʽ������ÿһ�����ӵ��˶�״̬����ͬ��
��3����̬ѹ����ΪҺ̬���������仯��Ũ��ˮ��������ȹܵ��Ƿ�й©�������백����Ӧ����NH4Cl�͵�������ѧ��Ӧ����ʽΪ��3Cl2+8NH3=6NH4Cl+N2��ClԪ�ػ��ϼ���0��-1�ۣ�NԪ�ػ��ϼ���-3�ۡ�0�ۣ�ת�Ƶ�����Ϊ6e-��
��4������Һ���е��ۣ�������Һ����ɫ���������궨��ˮ�еⵥ�ʵĺ����ﵽ�ζ��յ�ʱ��Һ����ɫ����ȥ���ݴ��жϣ����ݷ�Ӧ�ҳ���Ӧ��ϵʽ��Ȼ������������ݼ������ˮ�еⵥ�ʵ�Ũ�ȣ����ⶨֵ-����ֵ��������ֵ��100%���������
��� �⣺��1����ⱥ��ʳ��ˮ�����������ɡ�����������������ʽΪ��2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2�����ʴ�Ϊ��2NaCl+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$2NaOH+H2��+Cl2����
��2����ԭ�Ӻ��������Ϊ17����̬ԭ�Ӻ�������Ų�Ϊ1S12S22P63S23P5�������������Ų�ʽΪ3S23P5������ÿһ�����ӵ��˶�״̬����ͬ���������Ӻ�����18���˶�״̬��ͬ�ĵ��ӣ�
�ʴ�Ϊ��3S23P5��18��
��3����Ϊ��̬ѹ����ΪҺ̬���������仯����������ѹ����ΪҺ�����������仯�������백����Ӧ����NH4Cl�͵�������ѧ��Ӧ����ʽΪ��3Cl2+8NH3=6NH4Cl+N2��ClԪ�ػ��ϼ���0��-1�ۣ�NԪ�ػ��ϼ���-3�ۡ�0�ۣ�ת�Ƶ�����Ϊ6e-����˫���ű������ת�Ƶķ������Ŀ��Ϊ ��
��
�ʴ�Ϊ�������� ��
��
��4������Һ���е��ۣ�������Һ����ɫ�������������궨��ˮ�еⵥ�ʵĺ������жϴﵽ�ζ��յ����������Һ����ɫ��Ϊ��ɫ�����ڰ�����ڲ���ɫ��
ȡ��һ�����κ͵����ε�ƽ��ֵ�����ı�������������56mL������5Cl2+I2+6H2O��10HCl+2HIO3����
5Cl2��I2
5 1
$\frac{56��10{\;}^{-3}}{22.4}$mol xmol
����x=$\frac{2.5��10{\;}^{-3}mol}{5}$=5��10-4mol��
�ʵ�ˮ�еⵥ�ʵ�Ũ��Ϊ$\frac{5��10{\;}^{-4}mol}{0.5L}$=1��10-3 mol/L���ٶ���ˮ��ʵ��Ũ��Ϊ1.02��10-3 mol/L����ʵ���������Ϊ$\frac{1.0��10{\;}^{-3}-1.02��10{\;}^{-3}}{1.02��10{\;}^{-3}}$��100%=-1.96%��
�ʴ�Ϊ����Һ����ɫ��Ϊ��ɫ�����ڰ�����ڲ���ɫ��1��10-3��-1.96%��
���� ���⿼���˵�ⷽ��ʽ����д����������Ų������˶���������ԭ��Ӧ����ʽ����ƽ���йصζ����㣬�Ѷ��еȣ��Ƕ�֪ʶ���ۺ����ú������Ŀ��飮

 ��У����ϵ�д�
��У����ϵ�д�| A�� | �ߴ��ȵľ��������Ʊ�����ܵȰ뵼�塢����оƬ���ά | |
| B�� | PM 2.5��ָ������ֱ���ӽ�2.5��10-6m�Ŀ��������ɢ�ڿ������γɽ��� | |
| C�� | ��ǿ�ʴ����ʱ��Ӧ���ô���ˮ��ϴ������2%������Һ��������Һϴ�������ˮ��ϴ�������������һ������ | |
| D�� | NH4Fˮ��Һ�к���HF�����NH4F��Һ���ܴ���ڲ����Լ�ƿ�� |
| A�� | ���ʱ��Ni��OH��2Ϊ���� | |
| B�� | �ŵ�ʱ��FeΪ������Ni2O3Ϊ���� | |
| C�� | ���������صĵ������Һ�ʼ��� | |
| D�� | ���ʱ��������ӦʽΪFe��OH��2+2e-=Fe+2OH- |
| A�� | ����кͷ�Ӧ | B�� | ʵ����������غͶ������������� | ||
| C�� | ����ȼ�շ�Ӧ | D�� | ʵ������H2�ķ�Ӧ |
| A�� | ԭ����ܽ�ȫ����ѧ��ת��Ϊ���� | |
| B�� | ԭ��صĸ���ʧ���ӣ�������ԭ��Ӧ | |
| C�� | ԭ��ع���ʱ���为�����ϲ������Ӳ������·�������� | |
| D�� | ԭ��صĵ缫һ��Ҫ�����ֲ�ͬ�Ľ������ |
| A�� | �����ʺ�����ʳƷ | B�� | �����Ǻ�����ʳƷ | ||
| C�� | ��֬������ʳƷ | D�� | ά���غ�����ʳƷ |
 ��ͼΪKNO3��NaCl���ܽ�����ߣ���ش��������⣺
��ͼΪKNO3��NaCl���ܽ�����ߣ���ش��������⣺