题目内容
20.下列离子组中一定能够大量共存的是( )| A. | 无色溶液中:Na+、Cl-、SCN-、Fe3+ | |
| B. | 碱性溶液中:Na+、AlO2-、Cl-、SO42- | |
| C. | 加入铝粉后产生氢气的溶液中:Ba2+、K+、NO3-、Al3+ | |
| D. | 无色溶液中:Na+、HCO3-、Cl-、OH- |
分析 A.铁离子与有色离子,铁离子与硫氰根离子反应;
B.碱性溶液中存在大量氢氧根离子,四种离子之间不反应,都不与氢氧根离子反应;
C.加入铝粉后产生氢气的溶液中存在大量氢离子或氢氧根离子,铝离子与氢氧根离子反应,硝酸根离子在酸性条件下与铝反应不会生成氢气;
D.碳酸氢根离子与氢氧根离子反应.
解答 解:A.Fe3+为有色离子,SCN-、Fe3+之间反应生成硫氰化铁,在溶液中不能大量共存,故A错误;
B.碱性溶液中存在大量氢氧根离子,Na+、AlO2-、Cl-、SO42-之间不反应,都不与氢氧根离子反应,在溶液中能够大量共存,故B正确;
C.加入铝粉后产生氢气的溶液为酸性或强碱性溶液,溶液中存在大量氢氧根离子或氢离子,Al3+与氢氧根离子反应,NO3-在酸性条件下具有强氧化性,与铝反应不会生成氢气,故C错误;
D.HCO3-、OH-之间发生反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”.

练习册系列答案
相关题目
10.下列有关物质应用正确的是( )
| A. | 氯气、明矾净水原理相同 | |
| B. | 过氧化钠、活性炭均可用于呼吸面具 | |
| C. | 硅胶和铁粉均可用于食品的防氧化 | |
| D. | 甲烷的氯代物均可作防火材料 |
11.化学与生产、生活、社会密切相关.下列说法中正确的是( )
| A. | 铅笔芯的原材料为铅,儿童使用铅笔时如果用嘴吮吸能够引起铅中毒 | |
| B. | “轻轨电车”是一种交通工具,当电车启动时,电车电刷与导线的接触点上由于摩擦会产生高温,因此接触点上的材料应该选用耐高温、能导电的物质,石墨恰好合适 | |
| C. | 为防止中秋月饼等富含脂质食品氧化变质,常在包装袋中放入生石灰 | |
| D. | 双氧水是绿色氧化剂,可作医疗消毒剂,说明H2O2对人体无害 |
15.某溶液中存在大量的Cl-、SO42-、H+.该溶液中还可能大量存在的离子是( )
| A. | OH- | B. | Ba2+ | C. | Na+ | D. | Ag+ |
12.下列有关化学用语的表示正确的是( )
| A. | N2的电子式: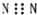 | |
| B. | 甲烷分子的比例模型是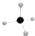 | |
| C. | 硝基和二氧化氮两种粒子所含电子数相等 | |
| D. | 中子数为10的氧原子:${\;}_{8}^{10}$O |
9.0.5mol 气态烃A 最多和1mol HCl加成,生成氯代烷B,1mol B与4mol Cl2 发生取代反应,生成只含碳、氯两种元素的化合物C,则A的分子式为( )
| A. | C2H4 | B. | C2H2 | C. | C3H4 | D. | C4H6 |
 有A、D、E、G、M、L六种前四周期的元素.A是宇宙中最丰富的元素.D原子核外有1个未成对电子,D+比E原子少一个电子层,E原子得一个电子填入3p轨道后,3p轨道呈全充满状态.G原子的2p轨道有2个未成对电子,M的最高化合价和最低化合价的代数和为4,与G的原子序数相差8.L位于周期表第12纵行且是六种元素中原子序数最大的.R是由M、L形成的化合物,其晶胞结构如图所示.请回答下列问题:
有A、D、E、G、M、L六种前四周期的元素.A是宇宙中最丰富的元素.D原子核外有1个未成对电子,D+比E原子少一个电子层,E原子得一个电子填入3p轨道后,3p轨道呈全充满状态.G原子的2p轨道有2个未成对电子,M的最高化合价和最低化合价的代数和为4,与G的原子序数相差8.L位于周期表第12纵行且是六种元素中原子序数最大的.R是由M、L形成的化合物,其晶胞结构如图所示.请回答下列问题: 非金属单质A和金属单质M可发生如图所示的转化关系,L的焰色是黄色,往L的溶液中加入稀盐酸和BaCl2溶液会生成白色沉淀.
非金属单质A和金属单质M可发生如图所示的转化关系,L的焰色是黄色,往L的溶液中加入稀盐酸和BaCl2溶液会生成白色沉淀.