题目内容
20.已知单质铁溶于一定浓度的硝酸溶液中反应的离子方程式为a Fe+b NO-3+c H+=d Fe2++f Fe3++g NO↑+h N2O↑+k H2O化学计量数a~k均为正整数,它们之间的关系错误的是( )| A. | c=4 g+10 h | B. | c-b=2 d+3 f | C. | 2 d+3 f=3 g+8 h | D. | a+c=d+f |
分析 根据N原子守恒推出b=g+2h①,由电荷守恒得c-b=2d+3f②,由得失电子相等得2d+3f=3g+8h③,
A.由②③得,c-b=3g+8h④,将①代入④得,c=4 g+10 h;
B.由②得,c-b=2d+3f;
C.由③得,2d+3f=3g+8h;
D.根据铁元素守恒,a=d+f.
解答 根据N原子守恒推出b=g+2h①,由电荷守恒得c-b=2d+3f②,由得失电子相等得2d+3f=3g+8h③,
A.由②③得,c-b=3g+8h④,将①代入④得,c=4 g+10 h,故A正确;
B.由②得,c-b=2d+3f,故B正确;
C.由③得,2d+3f=3g+8h,故C正确;
D.根据铁元素守恒,a=d+f,故D错误,
故选D.
点评 本题考查元素守恒,电荷守恒,得失电子守恒,在氧化还原反应方程式中的应用,本题难度中等.

练习册系列答案
相关题目
16.仅用提供的硅酸盐仪器(非硅酸盐仪器任选),不能达到相应实验目的是( )
| A. | 提纯粗盐:烧杯、玻璃棒、酒精灯、蒸发皿、漏斗 | |
| B. | 中和热的测定:量筒、温度计、环形玻璃搅拌棒、胶头滴管 | |
| C. | 用CCl4提取碘水中的碘:分液漏斗、烧杯 | |
| D. | 用18.4 mol•L-1浓硫酸配制100mL 1.0 mol•L-1硫酸:10mL量筒、烧杯、玻璃棒、100mL容量瓶、胶头滴管 |
8.下列实验装置、试剂选用或操作正确的是( )
| A. | 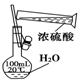 稀释浓硫酸 | B. | 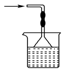 吸收氨气 | C. | 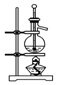 石油的分馏 | D. | 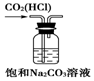 除去CO2中的HCl |
15.下列实验操作能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将NaOH浓溶液滴加到饱和的FeCl3溶液中 |
| B | 区分碳酸钠和碳酸氢钠两种溶液 | 用氢氧化钡溶液分别滴加,观察现象 |
| C | 除去Cu粉中混有的CuO | 加入稀硝酸溶液,过滤、洗涤、干燥 |
| D | CCl4萃取碘水中的I2 | 先从分液漏斗下口放出有机层,后从上口倒出水层 |
| A. | A | B. | B | C. | C | D. | D |
5.C(s)+H2O(g)═CO(g)+H2(g) △H=+131.3KJ/mol.它表示( )
| A. | 碳与水反应吸收131.3 KJ的热量 | |
| B. | 1mol固态焦炭与1mol水蒸气反应产生一氧化碳和氢气,吸收131.3 KJ的热量 | |
| C. | 1mol碳和1mol水反应吸收131.3 KJ的热量 | |
| D. | 固态碳和气态水各1mol反应,放出131.3 KJ的热量 |
9.下列说法正确的是( )
| A. | 氢氟酸、浓硝酸、硅酸钠溶液依次保存在棕色玻璃瓶、无色细口瓶、带胶塞细口瓶中 | |
| B. | 钠着火时不能用泡沫灭火器灭火 | |
| C. | 用饱和碳酸钠溶液除去CO2中混有的HCl | |
| D. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 |
10.下列说法准确的是( )
| A. | KNO3的溶解度高于NaCl | |
| B. | KNO3的溶解度低于NaCl | |
| C. | 含有多种杂质时,KNO3比NaCl更适合利用降温结晶(或重结晶)法进行提纯 | |
| D. | 含有多种杂质时,NaCl比KNO3更适合利用降温结晶(或重结晶)法进行提纯 |