题目内容
10.下列说法准确的是( )| A. | KNO3的溶解度高于NaCl | |
| B. | KNO3的溶解度低于NaCl | |
| C. | 含有多种杂质时,KNO3比NaCl更适合利用降温结晶(或重结晶)法进行提纯 | |
| D. | 含有多种杂质时,NaCl比KNO3更适合利用降温结晶(或重结晶)法进行提纯 |
分析 溶解度与温度有关,且硝酸钾的溶解度受温度影响大,而NaCl的溶解度受温度影响不大,以此来解答.
解答 解:由KNO3和NaCl的溶解度曲线图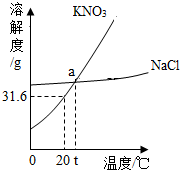 可知,
可知,
A.低温时KNO3的溶解度低于NaCl,故A错误;
B.温度较高时,KNO3的溶解度高于NaCl,故B错误;
C.硝酸钾的溶解度受温度影响大,而NaCl的溶解度受温度影响不大,则含有多种杂质时,KNO3比NaCl更适合利用降温结晶(或重结晶)法进行提纯,故C正确;
D.含有多种杂质时,NaCl比KNO3更适合利用蒸发结晶法进行提纯,故D错误;
故选C.
点评 本题考查混合物分离提纯,为高频考点,把握溶解度与温度的关系、溶解度的变化为解答的关键,侧重分析与应用能力的考查,注意结晶法的应用,题目难度不大.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
20.已知单质铁溶于一定浓度的硝酸溶液中反应的离子方程式为a Fe+b NO-3+c H+=d Fe2++f Fe3++g NO↑+h N2O↑+k H2O化学计量数a~k均为正整数,它们之间的关系错误的是( )
| A. | c=4 g+10 h | B. | c-b=2 d+3 f | C. | 2 d+3 f=3 g+8 h | D. | a+c=d+f |
1.在Ca(OH)2(Ksp=5.5×10-6)、Mg(OH)2(Ksp=1.2×10-11)、AgCl(Ksp=1.56×10-10) 三种物质中,下列说法正确的是( )
| A. | Mg(OH)2不能转化为Ca(OH)2 | B. | Ca(OH)2的溶解度最小 | ||
| C. | Ca(OH)2不能转化为 Mg(OH)2 | D. | Ksp越大,S不一定越大 |
18.下列说法正确的是( )
| A. | 容量瓶和分液漏斗使用前必须要检漏、干燥 | |
| B. | 可以用酒精萃取溶解在水中的碘 | |
| C. | 新制氯水应保存在棕色细口瓶中 | |
| D. | 某溶液焰色反应呈黄色,说明溶液中含有Na+,不含K+ |
5.下列有关有机物说法不正确的是( )
| A. | CH3CH(OH)CH2COOH系统命名法命名3-羟基丁酸 | |
| B. | 四苯基乙烯(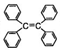 )中所有碳原子一定处于同一平面 )中所有碳原子一定处于同一平面 | |
| C. | lmol 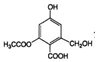 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol | |
| D. | 在一定条件下,苯与液溴、浓硝酸生成溴苯、硝基苯的反应都属于取代反应 |
15.某研究性学习小组查阅资料收集到如下信息:铁盐能蚀刻银而用来制作液晶显示器的银线路板.他们对蚀刻银的过程进行了探究.
【实验1】制备银镜:
(1)ⅰ.配制银氨溶液,需要的试剂是AgNO3溶液、稀氨水.并取等量银氨溶液于多支试管中.
ⅱ.向银氨溶液中加入等量的葡萄糖溶液,水浴加热.产生银镜,洗净,备用.
【实验2】溶解银镜:分别向两支试管中加入5mL Fe(NO3)3、Fe2(SO4)3溶液.
(2)选用Fe2(SO4)3溶液的浓度为0.05mol/L,目的是保证c(Fe3+)相等.
(3)从a、b中均检出了Fe2+,说明Fe3+具有氧化性.a中Fe3+氧化Ag的离子方程式
是Fe3++Ag═Fe2++Ag+.
(4)确认b中沉淀为Ag2SO4(微溶),检验Ag2SO4固体中SO42-的方法是取少量Ag2SO4固体于试管中,加入适量蒸馏水,振荡、静置,取上层清液,滴加Ba(NO3)2溶液,出现白色沉淀.
(5)推测在a中的酸性条件下NO3-氧化了银,证据是a中溶液黄色略变浅,b中溶液黄色明显变浅.通过如下实验验证了推测是合理的:
ⅰ.测pH:测定实验a中所用Fe(NO3)3溶液的pH=2;
ⅱ.配制溶液:配制pH=2,c(NO3-)=0.3mol/L的溶液.取5mL此溶液加入有银镜的试管,现象是银镜消失,溶液颜色无明显变化.
请将步骤ⅱ补充完整.
(6)分析a中白色沉淀的成分,提出假设.
假设1:Fe(OH)2; 假设2:AgNO2; 假设3:…
①设计实验方案验证假设1:取少量沉淀置于空气中,未变色.假设1不成立.
②设计实验方案验证假设2(已知:亚硝酸盐能与酸化的KI溶液反应).
【实验结论与讨论】铁盐能蚀刻银;NO3-能提高铁盐的蚀刻能力.推测硝酸铁溶液如果保持足够的酸性,可以避免产生沉淀.
【实验1】制备银镜:
(1)ⅰ.配制银氨溶液,需要的试剂是AgNO3溶液、稀氨水.并取等量银氨溶液于多支试管中.
ⅱ.向银氨溶液中加入等量的葡萄糖溶液,水浴加热.产生银镜,洗净,备用.
【实验2】溶解银镜:分别向两支试管中加入5mL Fe(NO3)3、Fe2(SO4)3溶液.
| 编号 | a | b |
| 试剂 | 0.1mol/L Fe(NO3)3 | 0.05mol/L Fe2(SO4)3 |
| 现象 | 银镜消失较快; 溶液黄色略变浅; 产生少许白色沉淀 | 银镜消失较慢; 溶液黄色明显变浅; 产生较多白色沉淀 |
(3)从a、b中均检出了Fe2+,说明Fe3+具有氧化性.a中Fe3+氧化Ag的离子方程式
是Fe3++Ag═Fe2++Ag+.
(4)确认b中沉淀为Ag2SO4(微溶),检验Ag2SO4固体中SO42-的方法是取少量Ag2SO4固体于试管中,加入适量蒸馏水,振荡、静置,取上层清液,滴加Ba(NO3)2溶液,出现白色沉淀.
(5)推测在a中的酸性条件下NO3-氧化了银,证据是a中溶液黄色略变浅,b中溶液黄色明显变浅.通过如下实验验证了推测是合理的:
ⅰ.测pH:测定实验a中所用Fe(NO3)3溶液的pH=2;
ⅱ.配制溶液:配制pH=2,c(NO3-)=0.3mol/L的溶液.取5mL此溶液加入有银镜的试管,现象是银镜消失,溶液颜色无明显变化.
请将步骤ⅱ补充完整.
(6)分析a中白色沉淀的成分,提出假设.
假设1:Fe(OH)2; 假设2:AgNO2; 假设3:…
①设计实验方案验证假设1:取少量沉淀置于空气中,未变色.假设1不成立.
②设计实验方案验证假设2(已知:亚硝酸盐能与酸化的KI溶液反应).
| 实验方案 | 预期现象和结论 |
20.可用来鉴别淀粉溶液、苯、乙酸的试剂是( )
| A. | 碘水 | B. | 氯化钠溶液 | C. | 氢氧化钠溶液 | D. | 溴水 |