题目内容
12.用以下三种途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;
②铜与稀硝酸反应;
③铜先跟氧气反应生成氧化铜,氧化铜再跟稀硝酸反应.
以下叙述中正确的是( )
| A. | 消耗铜的物质的量相等 | B. | 消耗硝酸的物质的量相等 | ||
| C. | 消耗铜的物质的量是①>②>③ | D. | 消耗硝酸的物质的量是①>②>③ |
分析 反应方程式分别为:①Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、②3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、③2Cu+O2=2CuO、CuO+2HNO3=Cu(NO3)2+H2O,根据方程式判断消耗硝酸的物质的量;根据原子守恒判断消耗铜的物质的量,据此进行解答.
解答 解:反应方程式分别为:①Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O、②3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O、③2Cu+O2=2CuO、CuO+2HNO3=Cu(NO3)2+H2O,根据方程式知,制取相同的硝酸铜需要硝酸的物质的量之比为12:8:6=6:4:3,所以消耗硝酸的量:①>②>③,故C错误、D正确;
根据铜原子守恒知,制取相同的硝酸铜时需要Cu的量相等,故A正确、B错误;
故选AD.
点评 本题考查化学实验方案方案的评价,题目难度中等,明确发生反应的实质为解答关键,注意掌握常见元素及其化合物性质,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑩十种元素在周期表中的位置.
(1)在这十种元素中,化学性质最不活泼的元素是氩 (填元素名称),金属性最强的元素符号是Mg (填元素符号),元素④的离子结构示意图是 ,①⑥⑦中原子半径最小的是C (填元素符号).
,①⑥⑦中原子半径最小的是C (填元素符号).
(2)元素④和⑨的气态氢化物中较稳定的物质是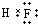 (填电子式)
(填电子式)
(3)⑤和⑨能以离子 (填化学键类型)键结合形成离子 (填晶体类型)晶体,溶解时破坏离子键 (填作用力类型).
(4)⑧和⑨离子的还原性比较⑧大于 ⑨(填大于、小于),最高价氧化物对应水化物的酸性更强的物质是HClO4 (填化学式)
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | =10 ⑩ |
 ,①⑥⑦中原子半径最小的是C (填元素符号).
,①⑥⑦中原子半径最小的是C (填元素符号).(2)元素④和⑨的气态氢化物中较稳定的物质是
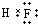 (填电子式)
(填电子式)(3)⑤和⑨能以离子 (填化学键类型)键结合形成离子 (填晶体类型)晶体,溶解时破坏离子键 (填作用力类型).
(4)⑧和⑨离子的还原性比较⑧大于 ⑨(填大于、小于),最高价氧化物对应水化物的酸性更强的物质是HClO4 (填化学式)
20.下列有关同分异构体数目的叙述中,不正确的是( )
| A. | 甲苯苯环上的一个氢原子被含4个碳原子的烷基取代,所得产物有12种 | |
| B. | 苯乙烯(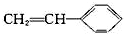 )和氢气完全加成的产物的一溴取代物有5种 )和氢气完全加成的产物的一溴取代物有5种 | |
| C. | 已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为3种 | |
| D. | 相对分子质量为106.5的一氯代烃,有8种同分异构体 |
7.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 28g氮气所含有的原子数目为NA | |
| B. | 标准状况下,22.4L水中含有个水分子NA | |
| C. | 2NA个氯气的体积是NA个氧气的体积的2倍 | |
| D. | 标准状况下,22.4L氯化氢所含的原子数为2NA |
17.用下列实验装置进行的实验中,能达到相应实验目的是( )
| A. | 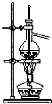 海水蒸馏 | B. | 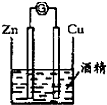 形成原电池 | C. | 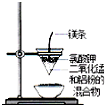 可制得金属锰 | D. | 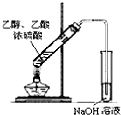 制取乙酸乙酯 |
4.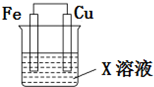 选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )
选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )
 选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )
选用下列试剂和电极:稀H2SO4、Fe2(SO4)3溶液、铁棒、铜棒、铂棒,组成如图所示的原电池装置(只有两个电极),观察到电流计G的指针均明显偏转(指针偏转程度大),则其可能的组合共有( )| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
1.下列说法不正确的是( )
| A. | 若0.5molCH4全部和Cl2发生取代反应,生成物质的量相等的四种有机物,则消耗Cl2的物质的量是1.25mol | |
| B. | 将CH3OH和分子式为C3H8O的醇混合,发生分子间脱水反应,可以得到的醚有6种 | |
| C. | 工业上要生产氯乙烷,用CH3CH3与Cl2发生取代反应制取比用CH2═CH2与HCl发生加成反应制取好 | |
| D. | 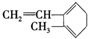 与Br2发生1:1加成反应,其加成产物最多有5种 与Br2发生1:1加成反应,其加成产物最多有5种 |
2.用0.1000mol•L-1的盐酸溶液滴定未知浓度的NaOH溶液时,下列操作正确的是( )
| A. | 装碱液的锥形瓶用NaOH溶液润洗 | |
| B. | 滴定时,眼睛注视酸式滴定管中液面的下降情况 | |
| C. | 应用右手控制酸式滴定管的活塞 | |
| D. | 若用甲基橙作指示剂,到滴定终点时锥形瓶内液体为橙色 |