题目内容
17.下列元素不属于主族元素的是( )| A. | 钙 | B. | 铜 | C. | 溴 | D. | 铯 |
分析 熟记常见元素在周期表中的位置,根据元素周期表的结构来判断元素所属的周期和族.
解答 解:A、钙元素在第ⅡA,属于主族元素,故A不选;
B、铜的外围电子排布为3d104s1,处于ds区,ⅠB族,故B选;
C、溴元素在第ⅥⅠA,属于主族元素,故C不选;
D、铯元素在第ⅠA,属于主族元素,故D不选.
故选B.
点评 本题考查学生元素在周期表中的位置以及周期和族的分布知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
10.既能与盐酸反应,又能与氢氧化钠溶液反应的有机物是( )
| A. | 氨基酸 | B. | 醋酸 | C. | 小苏打 | D. | 酒精 |
5.下图是某些难溶或微溶物在常温下的饱和溶液中的离子浓度关系,其中pM表示阳离子的物质的量浓度的负对数,而pR表示阴离子物质担的负对数,据此分析下列说法中正确的是( )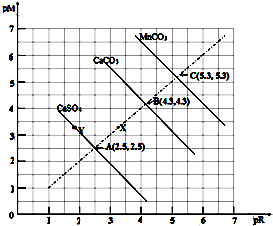

| A. | MnCO3在常温下的Ksp=2.5 x10-11(已知100.4=2.5) | |
| B. | 三种物质在常温下的溶解度大小顺序为MnCO3>CaCO3>CaSO4 | |
| C. | 处于Y点的CaSO4溶液中c(Ca2+)>c(SO42-) | |
| D. | Ca2+、CO32-浓度为X点的溶液可通过蒸发溶剂变为B点的溶液 |
12.(1)已知:①CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41kJ•mol-1
②C(s)+2H2(g)?CH4(g)△H=-73kJ•mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ•mol-1
则CO2(g)+4H2(g)?CH4(g)+2H2O(g)△H=-162kJ•mol-1.
(2)其他条件相同时,CO和H2按物质的量比1:3进行反应:CO(g)+3H2(g)?CH4(g)+H2O(g)
H2的平衡转化率在不同压强下,随温度的变化如图1所示.

①实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由与N点条件相比,选用M点条件时,虽然H2转化率低些,但温度较高,反应速率较快,压强为常压对设备要求不高,综合成本低.
②M点的平衡常数Kp=$\frac{\frac{0.9}{2.2}×1.01×1{0}^{5}×\frac{0.9}{2.2}×1.01×1{0}^{-5}}{\frac{0.1}{2.2}×1.01×1{0}^{-5}×(\frac{0.3}{2.2}×1.01×1{0}^{-5})^{3}}$.(只列算式.Kp的表达式是将平衡分压代替平衡浓度.某物质的平衡分压=总压×该物质的物质的量分数)
(3)如表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
①X、Y、C三种气体发生反应的化学方程式为Y+3X?2C.
②表中a的取值范围是25.1<a<64.2.
③根据如图3和上表分析,25min~40min内图中曲线发生变化的原因可能是缩小容器体积或增大压强;50min~65min内曲线发生变化的原因可能是增加C的物质的量或增大C的浓度.
②C(s)+2H2(g)?CH4(g)△H=-73kJ•mol-1
③2CO(g)?C(s)+CO2(g)△H=-171kJ•mol-1
则CO2(g)+4H2(g)?CH4(g)+2H2O(g)△H=-162kJ•mol-1.
(2)其他条件相同时,CO和H2按物质的量比1:3进行反应:CO(g)+3H2(g)?CH4(g)+H2O(g)
H2的平衡转化率在不同压强下,随温度的变化如图1所示.

①实际生产中采用图中M点而不是N点对应的反应条件,运用化学反应速率和平衡知识,同时考虑生产实际,说明选择该反应条件的理由与N点条件相比,选用M点条件时,虽然H2转化率低些,但温度较高,反应速率较快,压强为常压对设备要求不高,综合成本低.
②M点的平衡常数Kp=$\frac{\frac{0.9}{2.2}×1.01×1{0}^{5}×\frac{0.9}{2.2}×1.01×1{0}^{-5}}{\frac{0.1}{2.2}×1.01×1{0}^{-5}×(\frac{0.3}{2.2}×1.01×1{0}^{-5})^{3}}$.(只列算式.Kp的表达式是将平衡分压代替平衡浓度.某物质的平衡分压=总压×该物质的物质的量分数)
(3)如表示在一定条件下的1L的密闭容器中,X、Y、C三种气体因发生反应,三种气体的物质的量随时间的变化情况.表是3mol X和1mol Y在一定温度和一定压强下反应,达到平衡时C的体积分数(C%).
| 压强/MPa C% 速度/℃ | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.2 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
②表中a的取值范围是25.1<a<64.2.
③根据如图3和上表分析,25min~40min内图中曲线发生变化的原因可能是缩小容器体积或增大压强;50min~65min内曲线发生变化的原因可能是增加C的物质的量或增大C的浓度.
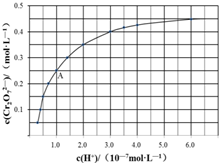 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题: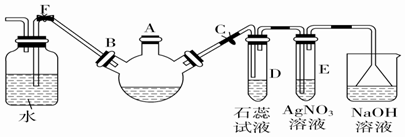
 .
.