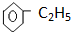题目内容
5.将氯气通入一定温度的氢氧化钾溶液中,得到含有次氯酸钾、氯酸钾和氯化钾的溶液,测得该溶液中c(ClO-):c(ClO3-)=2:1,则溶液中KCl和KClO的物质的量之比为( )| A. | 1:1 | B. | 2:5 | C. | 7:2 | D. | 2:7 |
分析 测得该溶液中c(ClO-):c(ClO3-)=2:1,设物质的量分别为2mol、1mol,生成KCl为ymol,结合电子守恒计算.
解答 解:测得该溶液中c(ClO-):c(ClO3-)=2:1,设物质的量分别为2mol、1mol,生成KCl为ymol,
由电子守恒可知,y×(1-0)=2mol×(1-0)+1mol×(5-0),
解得y=7mol,
则溶液中KCl和KClO的物质的量之比为7mol:2mol=7:2,
故选C.
点评 本题考查氧化还原反应的计算,为高频考点,把握Cl元素的化合价变化、电子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法应用,题目难度不大.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
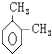
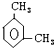
8.某有机物分子式为C4H8,据此推测其结构和性质均正确的是( )
| A. | 它与乙烯一定是同系物 | |
| B. | 它一定能使溴水褪色 | |
| C. | 它的一氯代物可能只有一种 | |
| D. | 等质量CH4和C4H8分别在氧气中完全燃烧,CH4的耗氧量小于C4H8 |
9.已知:RCH2OH$\stackrel{K_{2}Cr_{2}O_{7}/H+}{→}$RCHO$\stackrel{K_{2}Cr_{2}O_{7}/H+}{→}$RCOOH某有机物 X 的化学式为 C5H12O,能和钠反应放出氢气.X 经酸性重铬酸钾(K2Cr2O7)溶液氧化最终生成Y (C5H10O2),若不考虑立体结构.X和Y在一定条件下生成酯最多有( )
| A. | 32 种 | B. | 24 种 | C. | 16 种 | D. | 8 种 |
13.对于反应:M+N-→P,如果温度每升高10℃,化学反应速率提高到原来的3倍,在10℃时完成反应的10%需要81min,将温度提高到40℃时,完成反应的10%需要的时间为( )
| A. | 9 min | B. | 27 min | C. | 13.5 min | D. | 3 min |
20.向50mL14.0mol•L-1浓硝酸中加入足量的铜,充分反应后共收集到标准状况下2.24L NO和NO2混合气体(不考虑NO2与N2O4的相互转化),则参加反应的铜的质量为( )
| A. | 6.4g | B. | 12.8g | C. | 19.2g | D. | 38.4g |
17.一定条件下,一种反应物过量,另一种反应物仍不能完全反应的是( )
| A. | 过量的NaOH溶液与AlCl3溶液 | B. | 过量的浓盐酸与二氧化锰 | ||
| C. | 过量的铜与浓硫酸 | D. | 过量的锌与18 mol/L硫酸 |
14.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为2NA | |
| B. | 在反应KClO3+6HCl═KCl+3Cl2+3H2O中,每生成3molCl2转移的电子数为6NA | |
| C. | 含4molSi-O键的二氧化硅晶体中,氧原子数为2NA | |
| D. | 某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,生成SO3分子数为0.2NA |
15.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 能使紫色石蕊试剂变红的溶液中:NO3-、I-、Ba2+、Fe2+ | |
| B. | 含有大量Fe3+的溶液中:SCN-、I-、K+、Br- | |
| C. | pH=1的溶液中:K+、Br-、SO42-、Al3+ | |
| D. | 澄清石灰水中:Na+、K+、CH3COO-、HCO3- |