题目内容
现有等浓度的下列溶液,按溶液pH由小到大排列正确的是( )
①醋酸 ②碳酸钠 ③碳酸氢钠 ④碳酸 ⑤醋酸钠.
①醋酸 ②碳酸钠 ③碳酸氢钠 ④碳酸 ⑤醋酸钠.
| A、④①②⑤③ |
| B、④①②⑤③ |
| C、①④⑤③② |
| D、①④②③⑤ |
考点:盐类水解的应用,弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题,盐类的水解专题
分析:现按照溶液的酸碱性进行分组,再考虑电解质的强弱以及盐类水解的程度,可比较溶液的pH大小.
解答:
解:①④属于酸,由于醋酸酸性比碳酸强,则pH①<④,②③⑤均属于强碱弱酸盐,根据越弱越水解的原理知,因酸性:碳酸氢根<碳酸<醋酸,所以对应的盐其碱性为碳酸钠>碳酸氢钠>醋酸钠,即pH:⑤<③<②;
则按溶液pH由小到大排列正确的是①④⑤③②.
故选C.
则按溶液pH由小到大排列正确的是①④⑤③②.
故选C.
点评:本题考查弱电解质的电离和盐类的水解知识,题目难度不大,注意根据强酸、弱酸、水解呈酸性的盐、中性盐,水解呈碱性的盐、弱碱、强碱的顺序解答.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
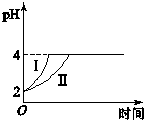 在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )
在常温下,取pH=2的盐酸和醋酸溶液各100mL.向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图( )| A、曲线Ⅰ表示盐酸的pH变化 |
| B、曲线Ⅱ表示盐酸的pH变化 |
| C、在相同条件下,两溶液生成的气体体积相等 |
| D、醋酸溶液中加入锌的质量比盐酸溶液中多 |
同种物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是( )
A、MnO2+4HCl(浓)
| ||||
| B、3Br2+6KOH═5KBr+KBrO3+3H2O | ||||
C、2KNO3
| ||||
D、NH4NO3
|
下列有关说法正确的是( )
| A、铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连 |
| B、用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 |
| C、一定温度下,反应2Mg(s)+CO2(g)=2MgO(s)+C(s)能自发进行,则该反应△H>0 |
| D、SO2(g)+2CO(g)?2CO2(g)+S(l)达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高 |
水溶液X中只可能溶有K+、Mg2+、Al3+、AlO2-、SiO32-、SO32-、CO32-、SO42-中的若干种离子.某同学对该溶液进行了如下实验:下列判断错误的是( )


| A、气体甲可能是混合物 |
| B、沉淀甲是硅酸和硅酸镁的混合物 |
| C、白色沉淀乙的主要成分是氢氧化铝 |
| D、K+、AlO2-和SiO3 2-一定存在于溶液X中 |
下列说法正确的是( )
| A、22.4L氧气中一定含有6.02×1023个氧分子 |
| B、18g水在标准状况下的体积是22.4L |
| C、标准状况下,20mL NH3与60mL O2所含的分子数之比为1:3 |
| D、金属元素只能存在于阳离子中 |
下列变化过程,属于放热反应的是( )
①水蒸气变成液态水
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸的电离.
①水蒸气变成液态水
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸的电离.
| A、②③④⑤ | B、②③④ |
| C、②⑤ | D、①②③④⑤ |
下列说法正确的是( )
| A、浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 |
| B、稀豆浆、云雾、淀粉溶液均为胶体 |
| C、直径介于1 nm~100 nm之间的微粒称为胶体 |
| D、布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分开 |