题目内容
13.在一定温度下,发生反应:Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g).已知该反应在不同温度下的平衡常数如下表:| 温度/℃ | 1000 | 1150 | 1300 |
| 平衡常数 | 64.0 | 50.7 | 42.9 |
(1)该反应的平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$,△H<0(填“<”、“>”或“=”)
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是B.
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡.求该时间范围内反应的平均反应速率v(CO2)=0.006 mol•L-1•min-1,CO的平衡转化率为60%.
(4)1000℃时,在(2)的平衡体系中,各加0.5molCO和0.5molCO2,v正>v逆(填“<”、“>”或“=”),平衡向正向移动(填“正向”、“逆向”或“不移动”).
分析 (1)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
由表中数据可知,随温度增大平衡常数减小,说明升高温度平衡逆向移动,则正反应为放热反应;
(2)提高CO的平衡转化率,应使平衡向正反应移动,但不能增大CO的用量,结合选项根据平衡移动原理分析;
(3)令平衡时CO的物质的量变化为nmol,则:
Fe2O3(s)+3CO(g)?Fe(s)+3CO2(g)
开始(mol):1 1
变化(mol):n n
平衡(mol):1-n n+1
所以$\frac{(n+1)^{3}}{(1-n)^{3}}$=64,解得n=0.6,
再根据v=$\frac{△c}{△t}$计算v(CO),转化率=$\frac{物质的量变化量}{起始物质的量}$×100%;
(4)计算此时浓度商Qc,若Qc=K,处于平衡状态,若Qc<K,反应向正反应进行,若Qc>K,反应向逆反应进行,进而判断v正、v逆的相对大小.
解答 解:(1)Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)的化学平衡常数表达式K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$;
由表中数据可知,随温度增大平衡常数减小,说明升高温度平衡逆向移动,则正反应为放热反应,故△H<0,
故答案为:$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$;<;
(2)A.升高温度,平衡常数减少,说明平衡逆向移动,CO的平衡转化率减小,故A错误;
B.移出部分CO2,平衡向正反应移动,CO的平衡转化率增大,故B正确;
C.加入催化剂,平衡不移动,故C错误;
D.减小体积,平衡不移动,故D错误.
故答案为:B;
(3)令平衡时CO的物质的量变化为nmol,则:
Fe2O3(s)+3CO(g)?Fe(s)+3CO2(g)
开始(mol):1 1
变化(mol):n n
平衡(mol):1-n n+1
所以K=$\frac{{c}^{3}(C{O}_{2})}{{c}^{3}(CO)}$=$\frac{(n+1)^{3}}{(1-n)^{3}}$=64,解得n=0.6,
v(CO2)=$\frac{\frac{0.6mol}{10L}}{10min}$=0.006 mol•L-1•min-1,
则CO的平衡转化率为$\frac{0.6mol}{1mol}$×100%=60%,
故答案为:0.006 mol•L-1•min-1;60%;
(4)浓度商Qc=$\frac{(1.6+0.5)^{3}}{(0.4+0.5)^{3}}$=12.7<K=64,反应向正反应进行,则v正>v逆,
故答案为:>;正向.
点评 本题考查化学平衡的有关计算、化学反应速率计算、平衡常数等,为高考常见题型,侧重于学生的分析能力和计算能力的考查,化学平衡移动原理分析判断是关键,题目难度中等.

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案(1)写出单质铁在水体中被(O2)氧化腐蚀得到水合氧化铁(FeOOH)的化学方程式:
4Fe+3O2+2H2O=4FeOOH.
(2)某课题组通过查阅文献,进行了用相同单质铁(相同性状和相同质量)在相同时间内,对影响单质铁去除一定量水体中砷的效率的因素提出了以下假设,并进行了实验探究:
假设1:水样的pH;
假设2:水体中所含其他物质及离子;
假设3:水体中的溶解氧;
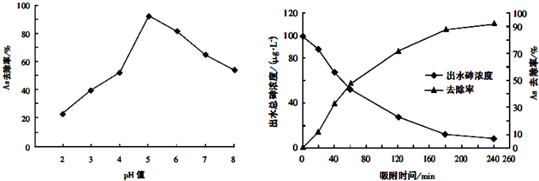
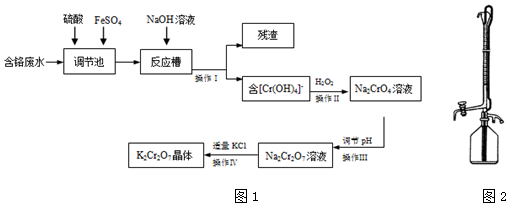
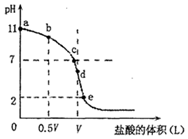
(3)其他条件相同,调节水样的pH,得到除砷效率曲线为图1,若控制水样pH=5时,测定不同时间段的除砷效率为图2:
①根据单质铁除砷原理,请解释水样酸性较强时,除砷效率较低的原因可能是酸性较强时,单质铁被腐蚀后,无法生成水合氧化铁,吸附能力下降,除砷效率降低;
②国家饮用水标准规定水中砷的含量应低于0.05mg/L(1mg=1000μg),根据图中信息判断:若控制水样的pH=6,出水后的砷浓度是否达到饮用水标准?达到.(填
“达到”、“未达到”或“无法判断”)
(4)为验证假设3,课题组成员设计了以下实验.请你完成表格中的内容(水样中砷的浓度可用分光光度计测定)
| 实验步骤 | 预期实验结果和结论 |
| ①取一定体积废水样品,分成体积相同两份,其中一份持续通入一段时间N2,以减少水中的溶解氧; | 若溶解氧不同的两份溶液中,测出的砷的浓度不同,则溶解氧对砷的去除效率有影响;反之则无影响. |
| ②向上述两份溶液中投入足量等质量的同种单质铁 | |
| ③相同一段时间后,用分光光度计测定两份水样中砷的浓度 |
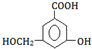
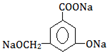
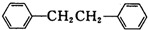 )是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:
)是一种重要的有机合成中间体,实验室可用苯和1,2一二氯乙烷(ClCH2CH2Cl)为原料,在无水AlCl3催化下加热制得,其制取步骤为:(一)催化剂的制备
下图是实验室制取少量无水AlCl3的相关实验装置的仪器和药品:

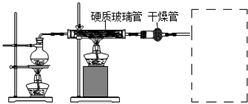
(1)将上述仪器连接成一套制备并保存无水AlCl3的装置,各管口标号连接顺序为:d接e,h接g,h接a,b接c.
(2)有人建议将上述装置中D去掉,其余装置和试剂不变,也能制备无水AlCl3.你认为这样做是否可行不可行(填“可行”或“不可行”),你的理由是制得的Cl2中混有的HCl与Al反应生成H2,H2与Cl2混合加热时会发生爆炸.
(3)装置A中隐藏着一种安全隐患,请提出一种改进方案:在硬质玻璃管与广口瓶之间用粗导管连接,防止AlCl3冷凝成固体造成堵塞.
(二)联苄的制备
联苄的制取原理为:
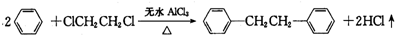
反应最佳条件为n(苯):n(1,2-二氯乙烷)=10:1,反应温度在60-65℃之间.
实验室制取联苄的装置如下图所示(加热和加持仪器略去):
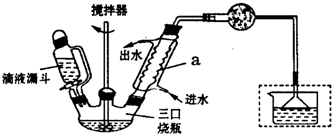
实验步骤:
在三口烧瓶中加入120.0mL苯和适量无水AlCl3,由滴液漏斗滴加10.7mL1,2-二
氯乙烷,控制反应温度在60-65℃,反应约60min.将反应后的混合物依次用稀盐酸、
2%Na2CO3溶液和H2O洗涤分离,在所得产物中加入少量无水MgSO4固体,静止、过
滤,先常压蒸馏,再减压蒸馏收集170~172℃的馏分,得联苄18.2g.
相关物理常数和物理性质如下表
| 名称 | 相对分子质量 | 密度/(g•cm-3) | 熔点/℃ | 沸点/℃ | 溶解性 |
| 苯 | 78 | 0.88 | 5.5 | 80.1 | 难溶水,易溶乙醇 |
| 1,2-二氯化烷 | 99 | 1.27 | -35.3 | 83.5 | 难溶水,可溶苯 |
| 无水氯化铝 | 133.5 | 2.44 | 190 | 178(升华) | 遇水分解,微溶苯 |
| 联苄 | 182 | 0.98 | 52 | 284 | 难溶水,易溶苯 |
(5)洗涤操作中,水洗的目的是洗掉Na2CO3(或洗掉可溶性无机物);无水硫酸镁的作用是吸水剂(干燥剂).
(6)常压蒸馏时,最低控制温度是83.5℃.
(7)该实验的产率约为72.85%.(小数点后保留两位有效数字)
| A. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| B. | 用蒸发的方法使NaCl从溶液中析出时,玻璃棒的作用是引流 | |
| C. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶的液面以下 | |
| D. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
 c(NH4+)+c(H+)=c(NH3•H2O)+c(OH-)
c(NH4+)+c(H+)=c(NH3•H2O)+c(OH-)
 .
. .
. .
.
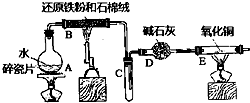 某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并进行了其他有关实验.(图中夹持及尾气处理装置均已略去)
某校化学小组学生利用如图所列装置进行“铁与水反应”的实验,并进行了其他有关实验.(图中夹持及尾气处理装置均已略去)