题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、澄清透明的溶液中:Na+、K+、MnO4-、AlO2- | ||
| B、0.1 mol?L-1 FeCl3溶液:K+、NH4+、I-、SCN- | ||
C、
| ||
| D、能溶解Al2O3的溶液:Na+、K+、Cl-、CO32- |
考点:离子共存问题
专题:
分析:A.四种离子之间不发生反应,且为澄清透明的溶液;
B.铁离子与硫氰根离子反应生成硫氰化铁;
C.该溶液为碱性溶液,铵根离子能够与氢氧根离子反应,次氯酸根离子能够氧化亚硫酸根离子;
D.能够溶液氧化铝的溶液为酸性或碱性溶液,碳酸根离子能够与氢离子反应.
B.铁离子与硫氰根离子反应生成硫氰化铁;
C.该溶液为碱性溶液,铵根离子能够与氢氧根离子反应,次氯酸根离子能够氧化亚硫酸根离子;
D.能够溶液氧化铝的溶液为酸性或碱性溶液,碳酸根离子能够与氢离子反应.
解答:
解:A.Na+、K+、MnO4-、AlO2-之间不发生反应,为澄清透明的溶液,在溶液中能够大量共存,故A正确;
B.Fe3+和 SCN-之间能够发生反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.该溶液中氢氧根离子浓度为0.1mol/L,溶液中存在大量氢氧根离子,NH4+与氢氧根离子反应,SO32-、ClO-之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.能溶解Al2O3的溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,CO32-与氢离子反应,在酸性溶液中不能大量共存,故D错误;
故选A.
B.Fe3+和 SCN-之间能够发生反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.该溶液中氢氧根离子浓度为0.1mol/L,溶液中存在大量氢氧根离子,NH4+与氢氧根离子反应,SO32-、ClO-之间发生氧化还原反应,在溶液中不能大量共存,故C错误;
D.能溶解Al2O3的溶液为酸性或碱性溶液,溶液中存在大量氢离子或氢氧根离子,CO32-与氢离子反应,在酸性溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存的判断,题目难度中等,明确离子反应发生条件为解答关键,注意掌握离子不能大量共存的常见情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;是“可能”共存,还是“一定”共存等.

练习册系列答案
相关题目
下列有关物质用途的说法中,正确的是( )
| A、氨气是生产硝酸的重要原料 |
| B、甲烷与氯气反应可制得纯净的一氯甲烷 |
| C、铁制容器可用来盛放稀硝酸 |
| D、油脂经皂化反应可获得高级脂肪酸 |
用电解水的方法分析水的组成时,需要加入一些电解质以增强水的导电性,其中不宜加入的物质是 ( )
| A、Na2SO4 |
| B、NaCl |
| C、CuSO4 |
| D、KOH |
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿按一定比例混合加热可制得铜:2CU2O+CU2S=6Cu+SO2↑.对于该反应,下列说法中正确的是( )
| A、该反应中的氧化剂只有Cu2O |
| B、氧化产物和还原产物的物质的量之比为1:6 |
| C、Cu既是氧化产物又是还原产物 |
| D、Cu2O在反应中既是氧化剂又是还原剂 |
高炉炼铁用于还原氧化铁的还原剂是( )
| A、一氧化碳 | B、焦炭 |
| C、石灰石 | D、空气 |
 为了比较温室效应气体对目前全球增温现象的影响,科学家通常引用“温室效应指数”,以二氧化碳为相对标准.表1有(A)至(I)共九种气体在大气中的体积百分比及其温室效应指数.
为了比较温室效应气体对目前全球增温现象的影响,科学家通常引用“温室效应指数”,以二氧化碳为相对标准.表1有(A)至(I)共九种气体在大气中的体积百分比及其温室效应指数.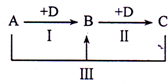 A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).