题目内容
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )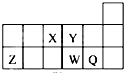

| A、元素X与元素Z的最高正化合价之和的数值等于7 |
| B、原子半径的大小顺序为:rZ>rW>rQ>rY>rX |
| C、离子Y2-和Z3+的核外电子数、电子层数和质子数都相同 |
| D、元素W的最高价氧化物对应的水化物的酸性比Q的弱 |
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素所在周期表中的位置可知,X为N元素,Y为O元素,Z为Al元素,W为S元素,Q为Cl元素,结合元素周期律的递变规律解答该题.
解答:
解:根据元素所在周期表中的位置可知,X为N元素,Y为O元素,Z为Al元素,W为S元素,Q为Cl元素,
A.X为N元素,最高正价为+5价,Z为Al元素,最高正价为+3价,则元素X与元素Z的最高正化合价之和的数值等于8,故A错误;
B.电子层结构相同,核电荷数越大,离子半径越小,电子层愈多,半径越大,rZ>rW>rQ>rX>rY,故B错误;
C.O2-、Al3+核外电子数都是10,电子层数都是2,质子数不相同,分别是8、13,故C错误;
D.同周期元素从左到右元素的非金属性逐渐增强,对应的最高价氧化物的水化物的酸性逐渐增强,则Q的最高价含氧酸的酸性较强,故D正确;
故选D.
A.X为N元素,最高正价为+5价,Z为Al元素,最高正价为+3价,则元素X与元素Z的最高正化合价之和的数值等于8,故A错误;
B.电子层结构相同,核电荷数越大,离子半径越小,电子层愈多,半径越大,rZ>rW>rQ>rX>rY,故B错误;
C.O2-、Al3+核外电子数都是10,电子层数都是2,质子数不相同,分别是8、13,故C错误;
D.同周期元素从左到右元素的非金属性逐渐增强,对应的最高价氧化物的水化物的酸性逐渐增强,则Q的最高价含氧酸的酸性较强,故D正确;
故选D.
点评:本题考查位置结构性质的相互关系及应用,难度中等,注意掌握元素周期表的结构和元素周期律的递变规律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列图象描述正确的是( )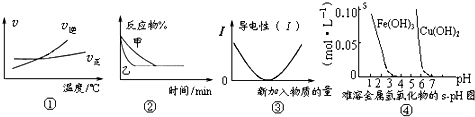

| A、根据图①可判断可逆反应“A2(g)+3B2(g)?2AB3(g)”的△H>0 |
| B、图②表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
| C、图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
| D、根据图④,若要除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO,至pH=4左右 |
实验室用MnO2与浓HCl制取Cl2:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,下列说法正确的是( )
| ||
| A、MnO2作氧化剂,发生氧化反应 |
| B、在反应中,表现还原性与表现酸性的HCl的物质的量之比为2:1 |
| C、每生成1mol Cl2时,有4mol电子发生转移 |
| D、氧化性:MnO2>Cl2 |
已知:①2Fe3++2I-=2Fe2++I2②2Fe2++Cl2=2Fe3++2Cl-③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O某溶液中含有Fe2+和I -,为了氧化I -而不使Fe2+被氧化,可选用的氧化剂是( )
| A、FeCl2 |
| B、KMnO4 |
| C、Cl2 |
| D、FeCl3 |
与3.2克SO2所含的氧原子数相等的NO2的质量为( )
| A、2.3 | B、4.6 |
| C、6.4 | D、3.2 |
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入6mol?L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
| A、60 mL |
| B、50 mL |
| C、30 mL |
| D、15 mL |
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A、1LpH=12的Ca(OH)2溶液中含阴离子0.02NA |
| B、标准状况下,NA个己烷分子所占的体积约为22.4 L |
| C、0.1mol氯气与足量的金属铁反应,转移的电子总数为0.3NA |
| D、20g重水(2H216O)含有的电子数为10NA |