题目内容
6.下列关于钠及其化合物的叙述正确的是( )| A. | Na在空气中久置最终变为过氧化钠 | |
| B. | 金属钠着火后应立即用泡沫灭火器灭火 | |
| C. | Na2O和Na2O2都是碱性氧化物 | |
| D. | Na2CO3叫纯碱,但属于盐类 |
分析 A、Na在空气中久置最终变为碳酸钠;
B、过氧化钠和二氧化碳反应生成氧气;
C、过氧化钠属于过氧化物;
D、Na2CO3叫纯碱,是由酸根离子与金属阳离子构成的化合物属于盐.
解答 解:A、Na在空气中被氧气氧化为氧化钠,氧化钠与水反应生成NaOH,再与二氧化碳反应生成碳酸钠,所以Na久置最终变为碳酸钠,故A错误;
B、过氧化钠和二氧化碳反应生成氧气,氧气助燃,所以金属钠着火后不能泡沫灭火器灭火,故B错误;
C、Na2O属于碱性氧化物,Na2O2是过氧化物,不是碱性氧化物,故C错误;
D、Na2CO3叫纯碱,在溶液中显碱性,Na2CO3是由碳酸根离子与钠离子构成的化合物属于盐,故D正确;
故选D.
点评 本题考查了钠及其化合物的性质,涉及钠和氧气的反应、过氧化钠、碳酸钠等知识点,有利于学生通过题目对有关知识进行归纳总结,掌握基础知识点即可轻松解题,题目难度不大.

练习册系列答案
相关题目
1.将白醋、食用油、食盐、酒精分别放入水中,不能形成溶液的是( )
| A. | 白醋 | B. | 食用油 | C. | 食盐 | D. | 酒精 |
1.乙苯催化脱氢制苯乙烯反应:

(1)已知:
计算上述反应的△H=+124 kJ•mol-1.
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{n{α}^{2}}{(1-{α}^{2})V}$(用含α等字母的代数式表示).

(1)已知:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能/kJ•molˉ1 | 412 | 348 | 612 | 436 |
(2)维持体系总压强p恒定,在温度T时,物质的量为n、体积为V的乙苯蒸汽发生催化脱氢反应.已知乙苯的平衡转化率为α,则在该温度下反应的平衡常数K=$\frac{n{α}^{2}}{(1-{α}^{2})V}$(用含α等字母的代数式表示).
18.下列4种分子,同种分子间不能发生化学反应的是( )
| A. | 乙烷 | B. | 乙醇 | C. | 氯乙烯 | D. | 丙烯 |
15.下列离子方程式正确的是( )
| A. | 亚硫酸氢铵溶液中滴加少量NaOH溶液:NH4++OH-═NH3.H2O | |
| B. | 酸性KI淀粉溶液久置后变蓝4I-+O2+2H2O═2I2+4OH- | |
| C. | 铜溶于稀硝酸中:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
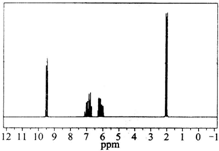 质谱图表明某有机物的相对分子质量为70,红外光谱表征到C═C和C═O的存在,1H核磁共振谱如图(峰面积之比依次为1:1:1:3):
质谱图表明某有机物的相对分子质量为70,红外光谱表征到C═C和C═O的存在,1H核磁共振谱如图(峰面积之比依次为1:1:1:3):