题目内容
【题目】下列叙述正确的个数是( )
①配位键在形成时,是由成键双方各提供一个电子形成共用电子对 ②s-s σ键与s-p σ键的电子云形状相同 ③Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]4s24p2,属于P区元素 ④非极性分子往往是高度对称的分子,比如BF3,PCl5,H2O2,CO2这样的分子 ⑤冰中存在极性共价键和氢键两种化学键的作用 ⑥Cu(OH)2是一种蓝色的沉淀,既溶于硝酸、浓硫酸,也能溶于氨水中 ⑦熔融状态的HgCl2不能导电,HgCl2的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgCl2是一种共价化合物、非电解质、盐 ⑧中心原子采取sp3杂化的分子,其立体构型不一定是正四面体形 ⑨键长:C-H<N-H<O-H ⑩第一电离能:Si<C<N<O<F
A. 1 B. 2 C. 3 D. 4
【答案】B
【解析】①配位键在形成时,含有孤电子对的原子提供电子、含有空轨道的原子提供轨道,二者形成配位键,故①错误;②S能级电子云是球形,P能级电子云是哑铃型,所以s-s σ键与s-p σ键的电子云形状不同,故②错误; ③根据最后排入电子名称确定元素在周期表中所属区名称,Ge是ⅣA族的一个主族元素,其核外电子排布式为Ge:[Ar]3d104s24p2,属于P区元素,故③错误;④H2O2结构为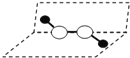 ,结构不对称,属于极性分子,故④错误;⑤冰中存在极性共价键和氢键两种作用,但氢键不是化学键,故⑤错误;⑥氢氧化铜能和硝酸、浓硫酸发生中和反应,溶于硝酸、浓硫酸,氢氧化铜能和氨水反应生成络合物离子银氨离子,所以氢氧化铜能溶于氨水中,故⑥正确;⑦HgCl2的稀溶液有弱的导电能力,可作手术刀的消毒液,是电离出的汞离子使蛋白质变性,说明其是弱电解质,故⑦错误;⑧中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体,如:水和氨气分子中中心原子采取sp3杂化,但H2O是V型,NH3是三角锥型,故⑧正确;⑨因C、N、O的原子半径依次减小,则键长:C-H>N-H>O-H,故⑨错误;⑩因N的2p轨道为半充满结构,相对稳定,则第一电离能:Si<C<O<N<F,故⑩错误;答案为B。
,结构不对称,属于极性分子,故④错误;⑤冰中存在极性共价键和氢键两种作用,但氢键不是化学键,故⑤错误;⑥氢氧化铜能和硝酸、浓硫酸发生中和反应,溶于硝酸、浓硫酸,氢氧化铜能和氨水反应生成络合物离子银氨离子,所以氢氧化铜能溶于氨水中,故⑥正确;⑦HgCl2的稀溶液有弱的导电能力,可作手术刀的消毒液,是电离出的汞离子使蛋白质变性,说明其是弱电解质,故⑦错误;⑧中心原子采取sp3杂化的分子,VSEPR模型是正四面体,但其立体构形不一定是正四面体,如:水和氨气分子中中心原子采取sp3杂化,但H2O是V型,NH3是三角锥型,故⑧正确;⑨因C、N、O的原子半径依次减小,则键长:C-H>N-H>O-H,故⑨错误;⑩因N的2p轨道为半充满结构,相对稳定,则第一电离能:Si<C<O<N<F,故⑩错误;答案为B。

【题目】某溶液中含有大量的Cl﹣、Br﹣、I﹣,若向1L该混合溶液中通入一定量的Cl2,溶液中Cl﹣、Br﹣、I﹣的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,原溶液中Cl﹣、Br﹣、I﹣的物质的量浓度之比为( )
Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
n(Cl﹣)/mol | 1.5 | 2.0 | 3.0 |
n(Br﹣)/mol | 3.0 | 2.8 | 1.8 |
n(I﹣)/mol | x(x>0) | 0 | 0 |
A. 5:15:4 B. 5:12:4
C. 15:30:8 D. 条件不足,无法计算




